UNIVERSITATEA PETROL - GAZE DIN PLOIESTI
FACULTATEA DE TEHNOLOGIA PETROLULUI SI PETROCHIMIE
CATEDRA I. P. P. P.
SPECIALIZAREA: PRELUCRAREA PETROLULUI, PETROCHIMIE SI CARBOCHIMIE
PROIECT DE DIPLOMA
TEMA: Proiectarea tehnologica a unei serpentine din cuptorul de piroliza al propanului
CAPITOLUL I
INTRODUCERE
Descompunerea sau tratarea termica a hidrocarburilor a inceput sa fie studiata inca din a doua jumatate a secolului al XIX-lea si a fost aplicata cu succes la scara industriala, in rafinarii, la inceputul secolului al XIX-lea.
Procesele industriale care au la baza descompunerea termica, dezvoltate in rafinarii, sunt: cocsarea (CX), cracarea termica (CT), reducerea de viscozitate (RV) si piroliza.
CX este o forma severa a cracarii termice avand ca scop reducerea cantitatii de combustibili de focare prin transformarea partiala a reziduurilor petroliere in produse mai usoare si cocs. Ulterior, o parte din cocsul de calitate a fost folosit pentru fabricarea electrozilor. Initial, procesul s-a realizat la presiuni ridicate, iar in prezent se aplica variantele: cocsare intarziata, cocsare in strat fluidizat si Flexicoking.
CT a avut ca scop initial producerea de benzina din fractiuni petroliere grele si reziduale,fiind ulterior total inlocuita, in acest sens, de cracarea catalitica. In prezent, revine in atentie, in principal pentru cracarea unor motorine, in scopul obtinerii gudroanelor puternic aromatice, corespunzatoare fabricarii cocsului acicular.
RV este o forma blanda a cracarii termice a reziduurilor de DV sau DA pentru producerea combustibililor reziduali cu viscozitati mici si obtinerea, in diverse proportii, a produselor mai usoare, care intra in fluxul de prelucrare al rafinariei.
Piroliza este cel mai important proces de descompunere termica avand ca scop principal fabricarea de olefine inferioare ( si in anumite cazuri a aromaticelor C6-C8 ), materii prime pentru industria petrochimica.
I.2.1. Mecanism de reactie
Cracarea termica a unei fractiuni petroliere are ca rezultat obtinerea unor produse cu puncte de fierbere mai mici si continut de hidrogen mai mare, precum si a produselor cu puncte de fierbere mai mari si continut de hidrogen mai mic decat al materiei prime. Din acest punct de vedere, cracarea termica apare ca o largire a intervalului de puncte de fierbere, insotita de o redistribuire a atomilor de hidrogen prin " transferul" lor de la moleculele hidrocarburilor mai grele catre acelea ale hidrocarburilor mai usoare. Cracarea termica este realizata uzual la temperaturi cuprinse intre 450°C si 850°C si la presiuni de la 1 bar la 75 bar, conditii in care au loc reactii de scindare a legaturilor C-C, de dehidrogenare, izomerizare, polimerizare. Cele mai importante sunt reactiile de descompunere termica. Exista o diferenta fundamental intre cracarea promotata numai termic si cea promotata termic in prezenta de catalizator, deoarece reactiile decurg dupa mecanisme diferite si, in consecinta, produsele obtinute au compozitii diferite.
Reactiile ireversibile, endoterme, de cracare a moleculelor parafinice sau a lanturilor laterale produc molecule cu mase moleculare mai mici, uzual o parafina si o olefina:
![]() R - CH 2 - CH2 - CH2
- R´ R - CH = CH2
+ R´- CH3
R - CH 2 - CH2 - CH2
- R´ R - CH = CH2
+ R´- CH3
Hidrocarburile olefinice se pot forma si prin reactia reversibila, deasemenea endoterma, de dehidrogenare a hidrocarburilor parafinice:
![]() R - CH2- CH3 R - C = CH2 + H2
R - CH2- CH3 R - C = CH2 + H2
Olefinele formate pot ele insele sa se descompuna sau sa dea urmatoarele tipuri de reactii:
Izomerizare ( usor endoterma) :
![]() CH3 - CH2 - CH =CH2 CH3 - CH = CH - CH3
CH3 - CH2 - CH =CH2 CH3 - CH = CH - CH3
Dehidrogenare ( endoterma ):
![]() CH3 - CH2 - CH =CH2 CH2 = CH - CH = CH2 +
H2
CH3 - CH2 - CH =CH2 CH2 = CH - CH = CH2 +
H2
Polimerizare ( exoterma ) :
![]() 2CH3
- CH2 - CH = CH2 CH3
- CH2 - CH2 - CH = CH- CH2-CH2-CH3
2CH3
- CH2 - CH = CH2 CH3
- CH2 - CH2 - CH = CH- CH2-CH2-CH3
Mecanismul postulat pentru reactiile principale ce au loc in procesele de cracare termica este acela al formarii radicalilor liberi care initiaza lantul de reactie. La temperaturile la care se desfasoara aceste procese are loc ruperea unei legaturi C- C ( 80 kcal/mol ) sau a unei legaturi C- H ( 98 kcal/mol).
Prin ruperea legaturii covalente apar doi radicali liberi primari, continand fiecare un singur electron, nepereche, care initiaza procesul in lant :
![]() R - CH2 - CH2 - CH2 - R´ R - CH2. + R´ - CH2 - CH2. sau
R - CH2 - CH2 - CH2 - R´ R - CH2. + R´ - CH2 - CH2. sau
![]() R - CH2 - CH2 - CH2 - R´ R - CH2 - CH - CH2 - R´+ H.
R - CH2 - CH2 - CH2 - R´ R - CH2 - CH - CH2 - R´+ H.
Odata formati primii radicali liberi, urmeaza propagarea reactiilor, cu formarea de noi radicali liberi, prin :
- radicalii secundari se pot rupe in pozitia β formand un nou radical primar mai scurt si o α-olefina :
![]() R - CH2 - CH . - CH2
- ´ R.+ R´ - CH2 - CH =
CH2
R - CH2 - CH . - CH2
- ´ R.+ R´ - CH2 - CH =
CH2
-ruperea legaturilor C - C in pozitia β fata de atomul de carbon care are electron impar, cu formarea unei olefine si a unui radical liber mai scurt :
![]() R - CH2 - CH2. R. + CH2 = CH2
R - CH2 - CH2. R. + CH2 = CH2
-radicalul liber cu masa moleculara mare poate extrage H. de la un atom de carbon propriu cu pozitia 5-6 spre centru, producand o rasucire a lantului parafinic si formarea unui nou radical liber.
Aceasta ipoteza asupra izomerizarii intramoleculare a radicalilor prin intermediul complecsilor de tranzitie ciclici, continand 5-6 atomi de carbon, este folosita pentru a explica randamentul superior de 1- hexena in descompunerea termica a n-C12H26.
In sfarsit, lantul de reactii poate fi intrerupt prin reactii intre radicali :
![]() .CH3
+ CH3 - CH2. CH3
- CH2 - CH3
.CH3
+ CH3 - CH2. CH3
- CH2 - CH3
![]() CH3 - CH2. + H . CH3 - CH3
CH3 - CH2. + H . CH3 - CH3
Hidrocarburile alchil-naftenice si alchil aromatice pierd lanturile alchilice printr-un mecanism similar. La temperaturi ridicate poate avea loc ruperea inelului naftenic sau pot avea loc reactii de dehidrogenare la inele naftenice nesaturate sau la hidrocarburi aromatice.
La cracarea termica a hidrocarburilor grele se pare ca, alaturi de mecanismul radicalic in lant, o pondere importanta o are si mecanismul molecular. Astfel, la cracarea 1-dodecenei si a 1-tetradecenei, formarea cu randamente foarte ridicate a α-olefinelor, avand cu trei atomi de carbon mai putin decat hidrocarbura supusa cracarii ( 1 - C9H18 si 1- C11H22 ), nu poate fi explicata satisfacator prin mecanismul radicalic in lant.
Un interes deosebit il prezinta mecanismul reactiilor care conduc in procesele de descompunere termica la formarea produselor mai grele decat materia prima, tinand seama de implicatiile acestora asupra ciclurilor de functionare ale instalatiilor, precum si asupra distributiei produselor de reactie. In cazul descompunerii termice a reziduurilor, imbogatirea respectiv saracirea in hidrogen a produselor cracarii fata de materia prima poate fi reprezentata printr-o ecuatie generala de bilant de forma:
![]() ( CH1,4)m 0,6( CH2)m
+ 0,4( CH0,5)m
( CH1,4)m 0,6( CH2)m
+ 0,4( CH0,5)m
Pe langa mecanismul postulat anterior, precum si diverse scheme propuse pentru ilustrarea formarii produselor foarte grele, o explicare a acestui "transfer" de hidrogen intre produsele mai grele si cele mai usoare in cracarea termica este data in cele ce urmeaza.
O analiza mai ampla privind locul ruperii moleculelor de hidrocarburi si nehidrocarburi continute in titei, a naturii radicalilor formati si modului de descompunere al acestora, se poate face pe baza cunoasterii valorilor energiilor de disociere ale diverselor legaturi interatomice. De exemplu, cunoasterea vitezelor relative de rupere ele diverselor legaturi interatomice si a unui mecanism de reactie pentru descompunerea unei hidrocarburi a permis calculul distributiei produselor de reactie la cracarea termica.
Studii de determinare a numarului de centrii paramagnetici ( radicali liberi) prin rezonanta paramagnetica a electronilor, in reziduul de vid, in reziduul de cracare catalitica, in reziduul de piroliza a benzinei si in asfaltenele separate din acestea arata ca asfaltenele contin de cel putin 5 ori mai multi radicali liberi pe unitatea de masa decat reziduul din care provin si ca prin cresterea severitatii cracarii creste concentratia de radicali liberi atat in reziduu cat si in asfaltenele corespunzatoare, cresterea fiind mai accentuata pentru acestea din urma, se poate deci admite ca gradul de nesaturare, exprimat prin concentratia de radicali liberi/mol in amestecul de reactie, este mai mare pentru componentele grele, putand conferi acestora caracter de "monomeri polifunctionali".
Pe de alta parte studiindu-se mecanismul reactiilor de polimerizare radicalica a monomerilor polifunctionali s-a constatat ca probabilitatea reactiilor de ciclizare intramoleculara creste o data cu viteza reactiei de initiere a polimerizarii. Totodata se stie ca viteza reactiilor de initiere a polimerizarii este direct proportionala cu concentratia de radicali liberi. Este deci de asteptat ca, in procesul de cracare termica, reactiile de recombinare a radicalilor liberi sa fie preponderent reactii de polimerizare liniara in domeniul fractiilor usoare, datorita concentratiei mici de radicali liberi si a caracterului preponderent monofunctonal al monomerilor si preponderent reactii de ciclizare intramoleculara in domeniul fractiilor grele, datorita concentratiei mari de radicali liberi si a caracterului polifunctional al monomerilor.
In acest mod devine explicit "transferul" de hidrogen de la hidrocarburile grele la cele usoare, acestea din urma formandu-se prin recombinarea radicalilor liberi usori rezultati si prin cracarea grupelor alchil din moleculele grele alchil-aromatice. Radicalii grei, cu concentratie mai mare de centrii paramagnetici, vor suferi preponderent reactii de ciclizare, rezultatul final al acestui proces complex fiind imbogatirea in hidrogen a fractiilor usoare de cracare si imbogatire in produsi de ciclizare aromatici a fractiilor grele.
I.2.2. Aspecte termodinamice
Studiul termodinamic al reactiilor care au loc in procesele chimice in general permite calculul caldurii de reactie, a entalpiei libere de reactie si a concentratiei teoretice maxime ( la echilibrul termodinamic) pe care ar putea-o atinge produsele in amestecul de reactie, in conditii date de temperatura si presiune, precum si interdependenta acestor factori.
In cazul proceselor de descompunere termica a fractiunilor petroliere complexe, calculele termodinamice au un caracter orientativ, care este determinat de complexitatea compozitiei materiei prime si a reactiilor ce pot avea loc, precum si de limitarile tehnologice impuse de obtinerea unor anumite produse dorite. Principalul criteriu de apreciere a posibilitatilor termodinamice de efectuare a reactiilor il reprezinta variatia entalpiei libere totale (∆G ) sau a entalpiei libere standard (∆G° ). Aceasta posibilitate poate fi utilizata fie examinand sensul variatiei acestui parametru cu temperatura [∆G = f (T)] fie prin stabilirea temperaturii pentru care ∆G =0, cand reactia devine posibila in ambele sensuri, iar K devine egal cu unitatea. Din examinarea variatiei cu temperatura entalpiei libere standard:
∆G° = -RT lnK
se poate aprecia, din punctul de vedere al compozitiei la echilibru, aplicabilitatea economica a procesului, la presiuni si temperaturi realizabile industrial. Pentru ∆G°=0, (la echilibru) rezulta valoarea corespunzatoare a temperaturii la acre reactia decurge spontan in conditii standard. Deoarece :
∆G° = ∆H - T∆S = -RT lnK
∆G° este variatia entalpiei libere standard a reactiei;
∆H - caldura de reactie ( negativa pentru reactii exoterme);
S - variatia entropiei de reactie;
K - constanta de echilibru;
R - constanta universala a gazelor = -1,987 cal/mol·K ; 8,314 J/mol·K
Daca valoarea lui ∆G° este negativa, valoarea lui K va fi relativ mare si randamentul va fi deasemenea mare cand echilibrul este atins. Daca ∆G° este apropiat de zero, valoarea lui K, si deci a randamentului, este mica. Daca ∆G° este relativ mare sau foarte mare, procesul nu este fezabil. Posibilitatea de aplicare industriala rezulta din calculul compozitiei la echilibru si din determinarea vitezei de reactie. In ecuatie, ∆G° poate fi determinat din entropii si calduri de reactie, din date de echilibru sau din corelatii ce permit calculul entalpiilor libere pentru diverse hidrocarburi.
Daca pentru calculul variatiei entalpiei libere a reactiei se utilizeaza variatiile entalpiei libere ale reactantilor si produsilor de reactie, atunci :
∆G° = Σ ∆G°produsi - Σ ∆G°reactanti
Caldura de reactie, ∆H, poate fi calculata pe baza entalpiilor standard de formare ( ∆Hf ) sau de combustie ( ∆Ha ) ale reactantilor si produsilor de reactie si a legii conservarii energiei :
∆H = Σ ∆Hf produsi - ΣH f reactanti
∆H = Σ ∆Ha reactanti - Σ∆Ha produsi
Pentru fractiuni petroliere lichide, caldurile de ardere se obtin in functie de densitate si de factorul de caracterizare. Factorul de caracterizare pentru fractiunile distilate se calculeaza in functie de temperatura medie de fierbere T si greutatea specifica, sau in functie de densitate si viscozitate. Caldurile de ardere sunt date la 60°C, in consecinta este necesara fie convertirea acestora la temperatura de cracare, fie convertirea caldurii de reactie de la 60°F la temperatura de cracare. Caldurile de reactie ale reactiilor endoterme sunt in functie de masele moleculare medii ale materiei prime ( Ma ) si produselor ( M p ) de reactie, pentru diverse procese si materii prime. In mod analog, caldura de reactie poate fi exprimata prin ecuatia :
∆H = 28000![]()
∆H se exprima in kcal/kg de materie prima, la 25°C si 1 bar.
Utilizarea, in scopuri orientative, a diverselor valori, diagrame corelatii empirice etc. date in literatura pentru estimarea caldurii de reactie in procesele termice, trebuie sa tina seama, printre altele, de modul de exprimare al acesteia.
I.2.3. Cinetica
Datele cinetice ale reactiilor chimice sunt utilizate la proiectarea reactoarelor industriale, pentru stabilirea conditiilor optime de operare din punct de vedere economic si al securitatii muncii.
Ca si in cazul abordarii aspectelor de mecanism de reactie si termodinamica, tratarile cinetice sunt conditionate de complexitatea reactiilor, a compozitiei materiei prime si a produselor etc., impunand o serie de ipoteze simplificatoare.
Estimarea cu o buna aproximatie a distributiei produselor de reactie, deci a efluentului, la iesirea din reactor constituie o conditie esentiala pentru o dimensionare corespunzatoare atat a reactorului cat si a sistemului de separare a produselor rezultate. Este clar ca in procesul de descompunere termica a hidrocarburilor au loc simultan reactii izolate, succesive si paralele, rezultand produse diverse conform ecuatiei :
![]() A ν1A1 + ν2A2 +
..+ νnAn
A ν1A1 + ν2A2 +
..+ νnAn
Mecanismul propus pentru aproximarea drumului parcurs de sistemul de reactie intre starea initiala si finala se exprima prin modelul cinetic al procesului pe baza caruia se formuleaza ecuatiile de bilant masic si de energie pentru fiecare component. Descomunerea termica a fractiunilor petroliere nu poate fi descrisa practic, din punct de vedere cinetic, prin componenti individuali, datorita complexitatii compozitiei acestora. Din aceasta cauza se recurge fie la modele cinetice globale, cu un singur pseudocomponent ( materia prima ), fie la definirea sistemului printr-un numar rezonabil de pseudocomponenti, grupati pe criteriul unei caracteristici comune, cum ar fi limitele de distilare pe curbe PRF, structura chimica etc.
Reactoarele tubulare industriale utilizate in procesele de descompunere termica aproximeaza destul de bine profilul ideal de curgere de tip piston, in consecinta variatia spatiala a parametrilor se va reprezenta prin ecuatii de bilant pentru volume infinitezimale ale sistemului, rezultand modele matematice formate din ecuatii diferentiale chiar in regim stationar de operare.
Modelul cinetic global
Acest model este de forma :
![]() A Produse si
serveste pentru a descrie viteza cu care materia prima A se transforma in
produse de reactie.
A Produse si
serveste pentru a descrie viteza cu care materia prima A se transforma in
produse de reactie.
Procesul global de descompunere termica poate fi descris satisfacator de o ecuatie cinetica de ordinul I :
![]() k ( 1 -
x ), de unde prin integrare k =
k ( 1 -
x ), de unde prin integrare k = ![]() , in care :
, in care :
x este conversia materiei prime dupa timpul τ;
τ este timpul de reactie, s; k este constanta vitezei de reactie, s-1.
Deoarece intr-un reactor industrial, temperatura creste dupa un anumit profil provocand variatii ale vitezei de reactie, evaluarea conversiei pe baza ecuatiei cinetice de mai sus se poate face prin simplificare, utilizand conceptul de "timp echivalent de sedere" la o temperatura specificata, T:
(τ ech)T= ![]()
Marimea ![]() ( sau pentru
procesul izoterm echivalent, produsul kτ) este utilizata ca o masura a
severitatii procesului, de cracare, definind o anumita conversie globala x;
este de precizat insa ca, la aceeasi severitate ( deci conversie globala ),
distributia produselor de reactie este mai mult sau mai putin functie de
valorile temperaturii si timpului de sedere, ceilalti parametrii ramanand
constanti.
( sau pentru
procesul izoterm echivalent, produsul kτ) este utilizata ca o masura a
severitatii procesului, de cracare, definind o anumita conversie globala x;
este de precizat insa ca, la aceeasi severitate ( deci conversie globala ),
distributia produselor de reactie este mai mult sau mai putin functie de
valorile temperaturii si timpului de sedere, ceilalti parametrii ramanand
constanti.
La conversii mari s-a constatat o scadere a vitezei de reactie fata de valoarea corespunzatoare, ecuatiei cinetice de ordinul I datorita "inhibarii" produsilor de reactie, ceea ce a condus la propunerea unor relatii cinetice de ordinul I ce tin seama de acest efect.
Principalul dezavantaj al modelului cinetic global, cu un singur psudocomponent ( materia prima ) este acela ca nu pot fi utilizate la estimarea distributiei produselor de reactie decat indirect, prin corelarea empirica a randamentelor de produse cu conversia globala a materiei prime. Din aceasta cauza s-a recurs la modele cinetice cu mai multi pseudocomponenti, acestia fiind, de regula, chiar produsele globale ale procesului.
I.2.4. Variabilele procesului
Presiunea
Un efect important al presiunii in reactorul unui proces de descompunere termica il constituie realizarea fazei in care au loc reactiile, afectand prin aceasta distributia produselor de reactie obtinute la cracarea unei materii prime date.
Presiunile scazute (2-8 bar) si temperaturile ridicate (600 - 850°C) se utilizeaza la cracari fara vapori (piroliza) si se favorizeaza obtinerea de hidrocarburi cu mase moleculare mici, C1 - C 4, cu randamente mari. La presiuni ridicate (15 - 75 atm) si temperaturi de 450 - 510°C se realizeaza procesele in faza mixta, care favorizeaza obtinerea cu prioritate a distilatelor usoare si medii alaturi de gudron si polimeri.
Temperatura
Constanta vitezei de reactie variaza cu temperatura conform unei ecuatii de tip Arrhenius:
k = A·![]() in care:
in care:
A - factorul de frecventa, s-1
E - energia de activare, kcal/mol
Reactiile de cracare termica ale hidrocarburilor incep practic la temperaturi de 315 - 370 °C, in functie de materia prima supusa cracarii.
Ca o
masura a influentei temperaturii asupra cracarii termice se utilizeaza uneori
numarul de grade (![]() ) cu care trebuie sa creasca temperatura pentru a dubla
viteza de reactie. Acest parametru poate fi utilizat in cazurile uzuale ale
proceselor de cracare termica a hidrocarburilor, care sunt neizoterme, pentru a
determina:
) cu care trebuie sa creasca temperatura pentru a dubla
viteza de reactie. Acest parametru poate fi utilizat in cazurile uzuale ale
proceselor de cracare termica a hidrocarburilor, care sunt neizoterme, pentru a
determina:
constanta vitezei de reactie k2 la temperatura t2 in functie de constanta k1 la temperatura t1 obtinuta in acelasi timp;
conversia globala x2 la o temperatura t2 si un anumit timp de sedere, in functie de conversia x1 la temperatura t1 obtinuta in acelasi timp;
timpul de sedere τ2 la temperatura t2 pentru o conversie data in functie de timpul de sedere τ1 la care se obtine aceeasi conversie;
cresterea conversiei (Δx) intr-un timp τ in care temperatura creste de la t0 la t1 cunoscand viteza de crestere a conversiei (x0) la temperatura t0 .
Materia prima
Datele privind variatia constantei vitezei de reactie cu temperatura pentru diverse materii prime (hidrocarburi pure sau fractiuni petroliere) permit sa se formuleze unele concluzii privind comportarea acestora la cracarea termica.
Constanta vitezei de reactie creste cu cresterea limitelor de distilare si a factorului de caracterizare al materiei prime, la aceeasi temperatura. Pentru produsele de cracare, constanta va fi mai mica decat pentru fractiuni necracate cu aceleasi limite de distilare. Pentru o materie prima data, supusa unui proces de descompunere termica, cunoasterea variatiei constantei vitezei de reactie cu temperatura (sau a constantelor cinetice A si -E) permite dimensionarea reactoarelor de CT, modelarea procesului si analiza performantelor acestora in exploatare
Timpul de sedere
Tinand
seama de faptul ca procesul global de descompunere termica este de ordinul I, o
anumita conversie x a materiei prime se poate obtine la o severitate k · ![]() sau
sau ![]() , deci timpul de sedere τ si temperatura t sunt din
punct de vedere al conversiei interschimbabile. Totusi, distributia produselor
de reactie este diferita. Evident, alegerea timpului de reactie la o
temperatura data se face in functie de produsul principal al carui randament
dorim sa il maximizam.
, deci timpul de sedere τ si temperatura t sunt din
punct de vedere al conversiei interschimbabile. Totusi, distributia produselor
de reactie este diferita. Evident, alegerea timpului de reactie la o
temperatura data se face in functie de produsul principal al carui randament
dorim sa il maximizam.
I.2.5. Realizarea industriala
Scopul procesului
La prelucrarea prin cracare termica a produselor petroliere grele si reziduale se urmareste diminuarea productiei de pacura si producere de distilate (motorina si benzina), iar, in unele cazuri, obtinerea de reziduu cu caracter aromatic pentru prelucrarile ulterioare. Cracarea termica se mai poate aplica si cu scopul de a reduce temperatura de congelare a motorinei din titeiuri parafinoase. Din proces rezulta in toate cazurile gaze cu un continut relativ ridicat de olefine C1-C4.
Distilatele de la cracarea termica se hidrofineaza si apoi se utilizeaza pe fluxul de prelucrare a produselor de distilare atmosferica. Gazele se prelucreaza prin absorbtie fractionare pentru separarea olefinelor C3-C4 materii prime pentru petrochimie.
Materii prime Asa cum s-a aratat, materiile prime supuse procesului de cracare termica sunt produse grele si reziduale: pacura DA, reziduul DV, motorine de CX si CC, extracte de ulei si chiar distilat de vid. In compozitia lor intra atat hidrocarburi saturate (parafine si nafteno-parafine) si nesaturate (alchil-aromatice, aromatice polinucleare), cat si compusi cu structuri de tip porfirinic.
Reactivitatea la cracarea termica a diverselor clase de hidrocarburi scade in urmatoarea ordine.
n-parafine>i-parafine>naftene>aromatice>aromatice polinucleare>rasini>asfaltene.
Deoarece reactiile de ciclizare si policondensare sunt de fapt reactii de intrerupere de lant, conditionate de existenta in mediul de reactie, in concentratie suficient de mare, de radicali liberi cu caracter polifunctional formati prin cracare termica, selectivitatea procesului de cracare catalitica se poate regla in anumite limite prin variatia parametrilor de reactie.
Astfel la cracarea pacurii DA si a reziduului de vid, obtinerea de maxim de distilate si minimizarea reactiilor de policondensare se asigura prin timp scurt de reactie, presiuni moderate si ratii de recirculare mari. In cazul cracarii motorinelor de cocsare si de cracare catalitica a extractelor sau a distilatului de vid in vederea obtinerii de reziduu aromatic pentru cocs acicular, procesul se realizeaza la temperaturi si presiuni (timp de reactie) mai mari.
Parametrii de operare. Valorile tipice ale parametrilor de operare sunt functie de materia prima supusa cracarii si de scopul urmarit.
pentru cracarea termica a pacurii DA si a reziduului DV, in schema cu doua
cuptoare (cracare selectiva), temperatura transferului cuptorului de cracare a
pacurii
(cuptorul greu) are valori de 480°C-490°C, temperatura transferului cuptorului
de
cracarea motorinei (cuptorul de cracare adanca sau cuptorul usor), 530-540°C,
presiunea
pe camera de reactie 18-20 at. Timpul de sedere (la rece) in serpentina
cuptoarelor este de
cea. 450 secunde pentru cuptorul greu si de cea. 950 secunde pentru cuptorul
usor.
pentru cracarea termica a motorinelor, in schema cu un singur cuptor,
temperatura transferului se situeaza in domeniul 540-550°C, timpul de sedere
(la rece) in
serpentina cuptorului cca. 950 secunde. Desigur ca valorile exacte ale
parametrilor se
determina pentru fiecare caz in parte functie de materia prima, conversia
impusa si scopul
prelucrarii.
Realizarea industriala, este prezentata in schema tehnologica tipica a unei instalatii de cracare selectiva cu doua cuptoare. In schema de proces cu doua cuptoare, rolul evaporatorului este de a permite o buna separare a reziduului de cracare de restul produselor distilate de cracare, deoarece pe la baza coloanei de fractionare se obtine fluxul de alimentare a cuptorului greu, constituit din materia prima amestecata cu fractia grea de produse recirculate. in tabelul 1.3. se prezinta caracteristicile tipice ale unor materii prime supuse la cracarea termica, precum si randamentele in produse si principalele caracteristici ale lor.
Caracteristicile tipice ale materiilor prime supuse la CT si randamentele in produse sunt prezentate in tabelul urmator:
Tabel I.1. Caracteristicile si randamentele in produse ale materiilor prime
|
|
Pacura DA |
Reziduu DV |
Amestec motorine CX si CC [45] |
|
A. Materii prime |
|
|
|
|
Cocs Conradson % |
|
|
|
|
Viscozitate °H/50°C |
|
|
|
|
Temp. initiala de fierbere, °C |
|
|
|
|
% Distilat la 360°C |
|
|
|
|
Factor de caracterizare UOP |
|
|
|
|
B. Randamente in produse Gaze |
|
|
|
|
Benzina final 200°C |
|
|
|
|
Motorina |
|
|
|
|
Reziduu |
|
|
|
I.3.1.Scopul procesului
Prin procesul de cocsare intarziata se obtin gaze, distilate usoare si medii, cu interval de fierbere intre 40 si 450°C, si cocs de petrol. Produsele lichide si gazele au caracter pronuntat nesaturat. O data cu cresterea ponderii titeiurilor sulfuroase si grele in productia mondiala de titei, urmata de cresterea productiei de pacura sulfuroasa, scopul procesului de cocsare s-a diversificat.
Se distinge astfel cocsarea materiilor prime cu continut redus de sulf (sub 1,5%) cu scopul producerii de cocs pentru mase anodice /cocs regular) si a cocsului pentru electrozi siderurgici (cocs acicular), cocsarea materiilor prime sulfuroase cand se urmareste producerea de distilate in detrimentul productiei de pacura sulfuroasa. In acest al doilea caz, cocsul sulfuros rezultat se utilizeaza drept combustibil la fabricarea cimentului sau la termocentrale, in amestec cu carbunele energetic etc.
I.3.2.Materiile prime
Materiile prime uzuale pentru instalatiile de cocsare intarziata sunt reziduul de DA si/sau DV cu continut de sulf determinat de utilizarea cocsului, asa cum s-a aratat mai inainte, si cu continut mic de cenusa.
I.3.3. Parametrii de operare.
Cocsarea intarziata se realizeaza la temperaturi (in camera de cocsare) de 460-480°C si presiuni de 3-5 atm. Temperatura materialului la iesirea din serpentina din radiatie a cuptorului de incalzire (materie prima + reciclu) se situeaza intre 485-500°C.
Temperatura in camera de cocsare este mai mica cu cca.25°C decat temperatura transferului datorita reactiilor endoterme de cracare si vaporizarii adiabate distilatelor in camera . Caderea de presiune pe cuptor (serpentina din radiatie) este de 10-11 atm. Raportul de recirculare (m. p + r/m.p.) 1,3 pina la 2,0.
I.4.1.Scopul procesului
RV este o cracare termica blanda a reziduurilor petroliere, in special a reziduului de vid, avand drept scop reducerea cantitatilor de combustibili reziduali, concomitent cu obtinerea unor fractiuni petroliere mai usoare (gaze, benzina, motorina).
I.4.2. Parametrii de operare
RV este un proces de descompunere termica usoara care se desfasoara la temperaturi de 450- 500°C si presiuni de 12-25 at. Materia prima este introdusa intr-un cuptor in care reactiile au loc partial sau total. Reactiile secundare tind sa duca la cocsarea serpentinei. De asemenea, cu cresterea conversiei, reziduul tinde sa devina instabil.
Procesele distructive aparute cu aproape 50 de ani in urma din nevoia maririi proportiei de fractiuni usoare obtinute din titei fata de continutul lor potential, ocupa un loc din ce in ce mai important in tehnologia prelucrarii titeiului. Importanta lor poate fi ilustrata de faptul ca in prezent capacitatea totala a instalatiilor de acest fel existente in lume, reprezinta mai mult de jumatate din capacitatea totala a instalatiilor de distilare primara.
Procesele distructive permit transformarea diverselor fractiuni de titei in componente indispensabile fabricarii combustibililor de motoare de calitate corespunzatoare exigentelor tehnicii moderne si asigurarii materiilor prime principale necesare industriei petrochimice.
Prin cracare termica si piroliza se intelege complexul de reactii ale hidrocarburilor sau fractiunilor de titei care au loc la temperaturi inalte, in conditiile in care reactiile de descompunere termica au un rol predominant.
Prin piroliza (cracarea la presiuni joase) se intelege in general procesele care au loc la presiuni joase (sub 5 atm) si temperaturi peste 650°C si al caror scop este obtinerea alchenelor inferioare si in cazuri mai rare a hidrocarburilor aromatice necesare industriei petrochimice. Datorita presiunii reduse, temperaturilor inalte si faptului ca materia prima se gaseste total in faza de vapori, in zona de reactie, in aceste procese lipsesc reactiile secundare de polimerizare. Practic, toata cantitatea de etena necesara industriei petrochimice se obtine prin piroliza. Orientativ, etena contribuie cu cca. 2/3 la tonajul monomerilor de baza ai produselor polimerice, la randul lor , acestia constituie cca. 70% din produsele de baza ale petrochimiei.
Piroliza se gaseste in concurenta cu procesele de cracare, indeosebi cu procesul de cracare catalitica, pentru productia de propena, butena si butadiena si cu procesul de reformare catalitica pentru productia de hidrocarburi aromatice. Mai mult de 3/4 din consumul de propena al industriei petrochimice provine din procesele de piroliza.
Evaluarea ponderii economice actuale a productiei instalatiilor de piroliza a hidrocarburilor in ansamblul industriei chimice si petrochimice se poate face, in prima aproximatie, luand in consideratie tonajul si valoarea produselor intermediare obtinute (olefine si hidrocarburi aromatice pure, fractiuni petroliere, etc). Evaluarea perspectivelor de evolutie in viitor a acestei productii este legata de posibilitatile de evaluare a necesitatilor de consum viitoare pentru o foarte mare diversitate de produse (plastomeri, elastomeri, fibre textile, produsi oxigenati, halogenati, etc).
Dezvoltarea unei industrii petrochimice incepe prin realizarea unor instalatii producatoare de materii prime specifice, cum sunt: piroliza unor fractii de titei pentru obtinerea olefinelor inferioare, reformarea metanului pentru fabricarea hidrogenului, productia si extractia aromaticelor, separarea butadienei, dehidrogenarea butanului si altele. Olefinele inferioare obtinute din instalatiile de piroliza reprezinta capatul de serie cel mai important. In conditiile diversificarii rapide a productiei de elastomeri si plastomeri nu se poate concepe realizarea unei productii industriale moderne fara introducerea in profilul de fabricatie al complexelor petrochimice, a unor instalatii de piroliza.
Consideratii economice bine cunoscute impun investitii considerabile pentru realizarea unor capacitati mari de productie si deci o competitie economica la scara pietii mondiale. Prognoza evolutiei productiei la aceasta scara va trebui sa tina seama si sa integreze ponderat un mare numar de factori specifici (tehnico-economici, de marketing, geografici, social).
I.5.1.Mecanism de reactie
Mecanismul reactiilor de piroliza si caracteristicile lor cinetice si termodinamice sunt similare reactiilor de cracare termica, reactii care au fost tratate anterior. S-a aratat ca prin reactiile in lant, prin mecanismul radicalilor liberi (Rice), se reuseste sa se prevada, cu o precizie apreciabila, compozitia produselor rezultate din piroliza oricarei hidrocarburi. In unele cazuri s-au observat totusi abateri remarcabile, care, in general cresc cu masa moleculara si cu complexitatea structurala a hidrocarburilor.
In piroliza, reactia primara consta in scindarea moleculelor de hidrocarburi alcanice in alcani si olefine. Aceasta este urmata de un complex de reactii succesive si paralele de cracare, de dehidrogenare, polimerizare etc.
Ruperea lantului in momentul initial are loc astfel:
o la alcani, are loc ruperea legaturilor C-C si nu C-H ; dintre legaturile C-C se vor rupe mai usor cele situate mai spre centrul moleculei si mai ales cele dintre carbonii cuaternari sau tertiari.
o
la alchene si alchine practic nu se produce ruperea dublei sau a triplei
legaturici a legaturilor C-H si a legaturii C-C vecine dublei sau a triplei
legaturi. Cel mai usor se va rupe legatura situata in pozitia ![]() fata de dubla legatura.
fata de dubla legatura.
o la alchil-aromatice practic nu va avea loc ruperea legaturii C-H, a legaturii din ciclu sau a legaturii dintre C aromatic si primul C al lantului lateral. Ruperea se va face de regula la legatura C-C din pozitia p fata de ciclu.
o pentru alchil cicloalcani, au loc ruperi C-C din lanturi laterale. In cazul hidrocarburilor cu lanturi laterale scurte sunt insa posibile si ruperi ale ciclului.
o ruperea se face usor la izoalcani, alcani superiori precum si hidrocarburi ciclice saturate si aromatice cu lanturi laterale lungi, decat la celelalte hidrocarburi.
Durata de existenta a radicalilor alchilici in general e foarte scurta. Pentru radicali CH3 · sau C2H5· este cuprinsa intre 1 · 10-3 -5 · 10 -3 s, la temperatura de 600-900°C si presiunea de lmmHg. In general ea scade cu cresterea temperaturii si a masei moleculare. Din cauza concentratiei lor mici, ciocnirea celor doi radicali, care duce la intreruperea lantului de reactie este mult mai putin probabila decat ciocnirea radicalilor cu moleculele nedescompuse.
Gradul in care radicalii cu masa moleculara mare se descompun cu formarea de produse cu masa moleculara mica inainte de a avea loc ciocnirea cu o molecula nedescompusa influenteaza compozitia produselor finale, deoarece ciocnirea cu alta molecula depinde de concentratie, in timp ce descompunerea radicalilor este independenta de concentratie.
Radicalii vor suferi o descompunere cu atat mai avansata cu cat concentratia hidrocarburilor in zona de reactie este mai mica. Deci in procesul de piroliza ( presiune mica si temperatura inalta ), radicalii se descompun si se obtine produsul final cu masa moleculara mai mica.
In general, viteza reactiilor de cracare devine intensa peste 700°C ( energia de legatura C - C este de cca. 83 kcal/mol, cea a legaturii C - H de cca. 100 kcal/mol), iar policondensarile cu formare de cocs spre 900°C. Timpul lung de reactie si temperatura scazuta favorizeaza polimerizarea olefinelor a diolefinelor si a acetilenelor. Reactivitatea in fiecare clasa de hidrocarburi creste cu masa moleculara.
Stoechiometric, reactiile pot fi incadrate in unul din urmatoarele 3 tipuri:
![]()
![]() A B +
C
A B +
C
![]()
![]() A + B C + D
A + B C + D
![]()
![]() A + B C
A + B C
Exprimate molecular, reactiile care duc la obtinerea de produse dorite sunt de tipul I, iar cele care duc la produse secundare, nedorite, sunt de tipul II sau III. Reactiile globale de dehidrogenare a parafinelor apartin tipului I.
S-a stabilit experimental ca energiile de activare ale reactiilor de tipul I au valori mult mai mari decat energiile de activare ale celor de tipul II sau III. Ca urmare, cresterea temperaturii duce la cresterea mai mare a valorilor constantelor de viteza ale reactiilor de tipul I ( in sensul de la stanga spre dreapta), in comparatie cu ale celorlalte tipuri.
Radicalii liberi formati prin ruperea legaturilor C-C cedeaza sau extrag cu mai multa usurinta atomii de hidrogen mai reactivi, diferenta in reactivitate scazand cu cresterea temperaturii.
Distributia produselor primare de reactie este determinata in mare masura de vitezele relative cu care reactioneaza atomii de hidrogen legati de atomii de carbon primari, secundari si tertiari ai materiei prime.
Hidrocarburile liniare contin numai atomi de hidrogen legati la atomii de carbon primari si secundari. Distributia produsilor rezultati din aceste hidrocarburi este relativ mai putin influentata de temperatura, deoarece variaza mai putin reactivitatea relativa a atomilor de hidrogen legati de atomii de carbon secundari si primari.
In cazul hidrocarburilor ramificate, temperaturile joase favorizeaza formarea olefinelor ramificate. Temperaturile inalte sunt cele care favorizeaza formarea de olefine usoare (etena, propena) in proportii marite, intrucat diferentele de reactivitate intre atomii de hidrogen, legati de atomii de carbon primari, secundari si tertiari scad cu cresterea temperaturii.
I.5.2. Termodinamica reactiilor de piroliza
Din analiza termodinamicii reactiei de piroliza se pot obtine trei categorii principale de informatii:
efecte termice ale transformarii moleculare ca atare sau ale ruperii unor legaturi intramoleculare
stabilitatea hidrocarburilor in raport cu conditia exterioara de temperatura, presiune, etc.
echilibrul reactiilor, singulare sau simultane, ale componentilor participanti la piroliza.
In procesele de piroliza intereseaza evaluarea efectelor termice ale reactiilor participante. Pentru calculul acestora este necesar sa se dispuna de entalpia standard de formare din elemente a reactantilor si produsilor reactiilor respective.
Cu exceptia H2O si CO2 pentru care caldura de formare se poate determina masurand caldura de sinteza direct din elemente, pentru celelalte substante care intervin in procesul de piroliza caldurile de formare din elemente se determina din caldurile de combustie, masurate calorimetric, ale tuturor participantilor la reactie.
In termodinamica chimica se iau ca valori standard ale parametrilor sistemului temperatura de 25°C si presiune absoluta de 1 atm.Cand reactia se desfasoara la presiune constanta variatia entalpiei ΔH0 se numeste de obicei caldura de reactie.
Caldura de reactie se poate determina experimental adica prin masurarea cantitatii de caldura in conditiile de lucru ale procesului.
![]()
Caldura de reactie ΔH poate fi negativa sau pozitiva dupa reactia exoterma sau endoterma. In procesul de piroliza, caldura are valoare pozitiva. Calculul randamentelor de echilibru din date termodinamice poate fi deosebit de util pentru hidrocarburi singulare C1- C3 .
Pentru fractiuni petroliere insa, sau chiar pentru hidrocarburi cu masa moleculara ridicata, interactiile reactanti - produsi devin atat de numeroase si variate incat efortul de a calcula conditiile de echilibru in piroliza, pentru randamente optime, devine practic iluzoriu.
I.5.3. Cinetica procesului de piroliza
Studiul cinetic este necesar pentru a cunoaste ordinul de reactie, pentru elaborarea ecuatiei cinetice necesare pentru calculul dispozitivului de reactie.
Diversitatea valorilor publicate pentru parametrii cinetici ai reactiilor de piroliza a hidrocarburilor este considerabil de mare astfel incat interpretarea lor presupune cunoasterea metodei de calcul prin care au fost obtinute, precum si conditiile experimentale de determinare.
In lucrarile in care procesul de piroliza este privit ca o reactie globala de ordinul 1, se utilizeaza pentru calculul constantei de viteza relatia de forma:
k =![]()
in care :
τ este timpul de sedere, s
x este conversia materiei prime
k este constanta de viteza a reactiei, s-1
Deoarece relatia de mai sus nu
descrie intotdeauna in mod satisfacator procesul de piroliza, intrucat s-a
constatat ca valoarea constantei de viteza astfel calculata scade cu conversia,
a fost necesara introducerea unui factor de franare ![]() care sa compenseze scaderea
constantei de viteza cu conversia.
care sa compenseze scaderea
constantei de viteza cu conversia.
k = ![]()
Potrivit
datelor publicate de A.Frost, valoarea factorului de franare pentru unele
hidrocarburi variaza in limitele 0,82 ![]()
Concluzie :
In general reactia de piroliza poate fi descrisa de ecuatii de viteza de ordin 1, ½, 2. De cele mai multe ori, ordinul global se atribuie reactiei ce exprima viteza de disparitie a reactantului.
Variatia vitezelor globale de piroliza determinate experimental se situeaza in succesiunea :
iC4H10![]() nC4H10
nC4H10![]() neoC5H12
neoC5H12![]() C
C![]() H8
H8![]() C2H6
C2H6
pe cand variatia constantelor de viteza pentru reactiile de initiere determinate de V. Tsang (1964) se situeaza astfel:
neoC5H12 ![]() nC4H10
nC4H10
![]() iC4H10
iC4H10 ![]() C3H8
C3H8 ![]() C2H6
C2H6
I.5.4.Variabilele de proces
Distributia produselor de reactie in cursul procesului de piroliza pentru un anumit tip constructiv de cuptor este functie de natura materiei prime si de conditiile in care are loc reactia de piroliza, respectiv de variabilele de proces.
Variabilele procesului de piroliza ar putea fi impartite in doua grupe mari si anume:
unele care determina repartitia produselor de reactie si deci economicitatea procesului
altele care afecteaza, in special, proiectarea cuptorului de reactie.
Din prima categorie fac parte: temperatura, respectiv profilul de temperatura in lungul serpentinei de reactie,timpul de sedere in zona de reactie, raportul abur/materie prima, presiune de iesire din zona de reactie si pierderea de presiune in lungul serpentinei.
Din grupa a doua fac parte: viteza de masa, lungimea totala a serpentinei, diametru interior al tevii, incarcarea termica, temperatura maxima a peretelui tevii, etc.
Odata proiectat si construit un cuptor de piroliza, repartitia produselor de reactie pentru o materie prima data este functie numai de anumite variabile asupra carora se poate actiona in cursul operarii procesului. Aceste variabile sunt: temperatura de intrare si iesire din zona de reactie, raportul abur/materie prima, presiunea de iesire.
Alte variabile cum sunt: timpul de sedere, presiunea medie, respectiv caderea de presiune sunt determinate prin proiect (debit de alimentare, diametru tevii, lungimea serpentinei), si nu pot fi variate decat in limite relativ inguste.
Functia cinetica de severitate
Pentru amestecuri complexe de hidrocarburi severitatea de cracare trebuie sa reflecte, ca si in cazul hidrocarburilor individuale, interdependenta dintre temperatura de reactie si timpul de sedere. Zdonik si colaboratorii sai au gasit o forma de exprimare a severitatii de cracare ca "functie cinetica de severitate' definita prin:
KSF=k5 dτ
unde:
KSF este functia cinetica de severitate
k 5-constanta vitezei de reactie pentru n-pentan, s-1
τ -timpul de sedere, s
Functia cinetica de severitate dupa conceptia autorilor este raportata la conversia n-pentanului.
A fost ales n-pentanul drept component de referinta, deoarece este in mod frecvent prezent in materia prima, cat si in produsele de reactie, dar nu se formeaza in cursul reactiilor de piroliza.Functia cinetica de severitate poate fi determinata direct pe cale experimentala, daca exista posibilitatea masurarii concentratiei relativ mici din aceasta hidrocarbura in alimentare si in efluent la iesirea din zona de reactie.
KSF=2,31og(c1/c2),unde:
c1 - concentratia n-pentanului in alimentare, % greutate
c2 - concentratia n-pentanului in efluent la iesirea din zona de reactie, %greutate.
Cu ajutorul functiei cinetice de severitate astfel definite se pot compara conversiile in produse obtinute in diferite conditii de piroliza.
Functia cinetica de severitate constituie o variabila de proces ce cuprinde interdependenta dintre doua variabile principale si anume: temperatura de reactie si timpul de sedere corespunzator cineticii reactiei. Ca atare este foarte utila in proiectare pentru o orientare asupra alegerii variantei optime de dimensionare a serpentinei de reactie.
In practica, operatorul poate varia severitatea de cracare actionand asupra temperaturii de iesire din zona de reactie.
Pentru determinarea functiei cinetice de severitate este necesara cunoasterea profilului de temperatura in lungul serpentinei de reactie si integrarea produsului k1·τ in vederea determinarii conversiei materiei prime la iesirea din zona de reactie, ceea ce se poate face practic cu ajutorul calculatorului.
Presiuna
In ceea ce priveste presiunea este importanta valoarea caderii de presiune prin zona de reactie a serpentinei si valorile presiunilor partiale ale hidrocarburilor, masurate prin produsul intre presiune totala si fractiile molare ale hidrocarburilor in amestec cu aburul.
Reactiile
de piroliza se efectueaza in tuburile zonei de radiatie a cuptoarelor ( in flux
stationar, in prezenta aburului, in conditii neizoterme si neadiabatice), la
presiuni de 2 - 4,5 bar, la temperaturi de 750 - 850![]() si cu timpi de
reactie medii de 0,05 la 0,5 s in cazul materiilor prime lichide si 0,5 - 1,2 s
pentru etan.
si cu timpi de
reactie medii de 0,05 la 0,5 s in cazul materiilor prime lichide si 0,5 - 1,2 s
pentru etan.
Deoarece reactiile de descompunere termica sunt ireversibile, influenta presiunii asupra desfasurarii lor nu poate fi efectuata pe baza termodinamica.
Fara a influenta viteza globala a acestor reactii, care au ordinul de reactie 1, presiunea influenteaza mecanismul lor. Cresterea presiunii mareste probabilitatea ciocnirii radicalilor cu o molecula nedescompusa, micsorand intervalul mediu de timp intre formarea radicalului si ciocnirea lui cu o molecula.In aceasta situatie, radicalii de masa moleculara mare vor avea in mai mica masura timpul necesar pentru a suferi toate scindarile succesive posibile. In consecinta, la presiuni mai mari se va forma o cantitate mai mica de produse de descompunere de masa moleculara mica.
Influenta presiunii de iesire asupra distributiei produselor
Presiunea de iesire din cuptor influenteaza distributia produselor de piroliza, in primul rand, datorita efectului ei asupra presiunii partiale a hidrocarburilor. Dar presiunea de iesire influenteaza, totodata, timpul de sedere ca urmare a efectului ei asupra densitatii amestecului gazos.
Pierderea de presiune in cuptor este legata de timpul constructiv al cuptorului si serpentinei de reactie (diametru, numar de serpentine in paralel, lungime, numar de coturi de intoarcere, etc). Tendinta este de a realiza pierderi de presiuni cat mai mici, astfel incat presiunea medie in serpentina de reactie sa nu depaseasca 2,7-3 atm. Aceasta se obtine prin scurtarea lungimii serpentinei, respectiv reducerea timpului de sedere. In acest caz capacitatea cuptorului se realizeaza prin montarea unui numar mare de serpentine in paralel. In acest fel, variatia diametrului urmareste, intr-o oarecare masura, variatia volumului specific, respectiv cresterea numarului de moli in lungul serpentinei.
Influenta presiunii partiale a hidrocarburilor asupra selectivitatii
Presiunea partiala a hidrocarburilor in amestecul de reactie influenteaza echilibrul chimic si viteza de reactie si in consecinta, distributia produselor de reactie.
In procesul de piroliza a hidrocarburilor, scaderea presiunii partiale a hidrocarburilor conduce la continuarea lanturilor radicalice, la cresterea cantitatilor de olefine si la micsorarea cantitatilor de produse de condensare. Totodata are loc si o crestere a raportului dintre acetilene si diolefine fata de monoolefine.
Raportul abur/materie prima
Aburul, ca agent de dilutie a hidrocarburilor, are urmatoarele functii:
reducerea presiuni partiale a hidrocarburilor, ceea ce se reflecta in cresterea selectivitatii procesului catre produsele mai valoroase, olefine inferioare.
scade presiunea partiala a hidrocarburilor aromatice cu punct de fierbere ridicat in zona conversiilor mari, micsorand astfel depunerile de cocs si prelungind ciclul de functionare intre doua decocsari.
ca urmare a unei conductibilitati termice ridicate mentine serpentina de reactie la un nivel mai coborat de temperatura in timpul reactiei endoterme.
oxideaza suprafata interioara a tevilor avand ca urmare diminuarea efectului catalitic al Fe si Ni, care favorizeaza reactiile de formare a carbonului.
Aburul, insa, reduce capacitatea cuptorului si sporeste consumul de utilitati intrucat el trebuie generat, supraincalzit, apoi condensat si racit.
Alegerea unui anumit raport abur/materie prima, respectiv a unei presiuni partiale date este functie de: presiunea de iesire din zona de reactie, greutatea moleculara a materiei prime supuse pirolizei si severitatea de cracare.
Raportul abur/materie prima este in stransa legatura si cu severitatea de cracare. Efectul lui se observa, mai ales in cazul materiilor prime grele. Astfel, in cazul pirolizei motorinei cu raport abur/materie prima 0,7 kg/kg la un timp de sedere de 0,5 s trebuie operat la o severitate de cracare redusa (temperatura de iesire 750-760°C).
Raportul abur/materie prima se calculeaza pentru conditiile de iesire din serpentina de reactie, deoarece pe aceasta ultima portiune conversiile sunt mai ridicate, iar tendinta de cocsare este mai accentuata.Acesta este cazul cuptoarelor de piroliza proiectate pentru o cadere mare de presiune (ΔP=l,5-2,0 atm.), presiunea partiala a hidrocarburilor trecand printr-un maxim care se situeaza la o oarecare distanta de iesirea din serpentina, punct in care conversiile sunt mai ridicate.
Temperatura
Conform cineticii reactiilor de formare a olefinelor,
conversia materiei prime este o functie de temperatura de reactie si timp de
sedere. O conversie data poate fi obtinuta cu un numar infinit de combinatii
ale temperaturii si timpului de sedere. La acelasi timp de sedere, cresterea
temperaturii conduce la marirea conversiei. In cuptoarele tubulare de piroliza
temperatura fluidului creste progresiv de la intrare in zona de radiatie pana
la iesirea din cuptor. La inceput temperatura creste rapid, materia prima
incalzindu-se pana la temperatura la care viteza reactiei de descompunere
devine substantiala. Apoi, temperatura creste monoton ca urmare a reactiilor de
piroliza endoterme. Cresterea rapida a temperaturii in zona conversiilor
ridicate nu este de dorit, intrucat fluxuri termice mari conduc la temperaturi
ridicate ale reactiilor secundare de formare a cocsului. Conditiile de ardere
trebuie astfel alese incat aportul de cadura sa fie usor in exces fata de
caldura ceruta de reactie.
Temperatura variaza in lungul unei serpentine de reactie date, dupa o curba
determinata de viteza de masa (kg /m2![]() ), de fluxul
termic specific ( kcal/ m2
), de fluxul
termic specific ( kcal/ m2![]() ) si de natura materiei prime. Pentru o curba de
incalzire si o serpentina data, timpul de reactie variaza cu natura materiei
prime si cu raportul abur/ materie prima. Temperatura se defineste uzual prin
valoarea acesteia la iesirea produsului din cuptor.
) si de natura materiei prime. Pentru o curba de
incalzire si o serpentina data, timpul de reactie variaza cu natura materiei
prime si cu raportul abur/ materie prima. Temperatura se defineste uzual prin
valoarea acesteia la iesirea produsului din cuptor.
Timpul
de reactie ![]() , se exprima convectional prin valoarea medie
corespunzatoare conditiilor de intrare, de cca 600
, se exprima convectional prin valoarea medie
corespunzatoare conditiilor de intrare, de cca 600![]() , si de iesire a amestecului de reactie din zona de
reactie a cuptorului.
, si de iesire a amestecului de reactie din zona de
reactie a cuptorului.![]() este timpul in
care reactia daca ar fi condusa izoterm ar produce aceeasi conversie a
produselor, asemanatoare celor obtinute in serpentina industriala.
este timpul in
care reactia daca ar fi condusa izoterm ar produce aceeasi conversie a
produselor, asemanatoare celor obtinute in serpentina industriala.
Profilul de temperatura este o caracteristica specifica unui anumit cuptor pentru o materie prima data. El se stabileste prin proiect in functie de geometria serpentinei de reactie, conditiile de ardere si dispunerea arzatoarelor. La un cuptor existent, profilul de temperatura nu poate fi modificat decat in limite foarte inguste prin ajustarea focului la arzatoare.
Influenta temperaturii asupra vitezei de reactie este data de relatia lui Arrhenius:
![]()
sau, sub forma integrata:
![]() ,unde:
,unde:
k - constanta vitezei de reactie
T - temperatura reactiei, in cal/mol
R=1,987 cal/mol - constanta gazelor
c - constanta de integrare
Pentru determinarea experimentala a energiei de activare, relatia de mai sus se integreaza intre doua limite T1 si T2, eliminandu-se astfel constanta de integrare c si obtinandu-se:
![]()
In practica industriala pentru caracterizarea masurii in care temperatura influenteaza viteza de reactie nu se foloseste energia de activare, ci alte doua notiuni care permit aprecierea directa a masurii in care temperatura influenteaza procesul. Aceste notiuni sunt: coeficientul de temperatura al vitezei de reactie kt, care reprezinta raportul constantelor vitezelor de reactie pentru doua temperaturi ce difera cu 10°C si gradientul de temperatura al vitezei de reactie a, care exprima numarul de grade cu care trebuie sa creasca temperatura pentru ca viteza de reactie sa se dubleze.
Legatura dintre coeficientul de temperatura al vitezei de reactie kt si energia de activare poate fi dedusa facand inlocuirile corespunzatoare definitiei lui kt in relatia de mai sus, astfel:
![]() de unde:
de unde:
![]()
Reactiile de piroliza au viteze masurabile in domeniul de temperaturi peste 600°C. Din aceasta cauza temperatura de intrare in zona de radiatie a cuptorului se limiteaza la 580-600°C.
Distributia produselor de reactie este influentata in mare masura de temperatura de iesire din zona de reactie. La acelasi timp de sedere si presiune partiala a hidrocarburilor, cresterea temperaturii de iesire are un efect favorabil asupra conversiei in etilena.
Un alt parametru utilizat in legatura cu relatia timp-temperatura este volumul echivalent de reactie, Ve , definit prin volumul unui reactor ipotetic, care, cu o materie prima data, ar produce, in conditii izoterme si izobare, la temperatura si presiunea partiala a hidrocarburilor la iesirea din reactorul real, aceeasi conversie cu a acestuia din urma.
Factorul materie prima
Materiile prime constau din: etan, propan, n- butan si amestecuri ale acestora: benzine primare, benzine hidrogenate provenite din procesele de cracare termica, motorine DA si DV, ca atare sau dezaromatizate si desulfurizate partial prin hidratare. Etanul constituie in general cea mai avantajoasa materie prima datorita randamentului de 80% in etena, productie redusa in derivati secundari, investitii reduse in instalatiile de fractionare a componentilor C3+ , cost convenabil pentru tarile cu o mare productie de titei, cost care, se reduce in unele cazuri la acela de recuperare, depozitare si transport al etanului. In unele din procesele de piroliza neconventionale se urmareste piroliza titeiului si a produselor reziduale rezultate din prelucrarea acestuia; in altele se produce etena prin reactii catalitice.
Materia prima se caracterizeaza prin continutul de componenti puri, in cazul alimentarii cu C2, C3, C4, sau cu amestecuri ale acestora. Pentru materiile prime lichide se determina uzual densitatea, curba de distilare, compozitia PONA, proprietatile spectrale si unii indici de caracterizare.
Alegerea materiei prime
Alegerea materiei prime in piroliza depinde de conditiile tehnico - economice concrete si anume:
o disponibilitatile existente tinand seama de utilizarea cea mai rationala pe ansamblu a diverselor fractiuni petroliere;
o produsele pe care piroliza urmeaza sa le furnizeze pentru diverse procese petrochimice;
o limitarile dictate de instalatia de piroliza.
Ultimul aspect se refera la faptul ca, in instalatiile de piroliza cu cuptoare tubulare, nu pot fi cracate fractiuni reziduale, din cauza formarii unor cantitati mari de cocs. Piroliza pacurei si a altor reziduuri este posibila numai in sisteme cu purtator de caldura solid, in care cocsul se depune pe purtator si este ars pentru reincalzirea acestuia, sisteme ce nu au fost insa puse la punct in suficienta masura pana in prezent, pentru a putea fi utilizate pe scara larga, realizarile existente limitandu-se la instalatii cu caracter experimental. De aici rezulta ca materiile prime ce pot fi practic folosite in prezent in piroliza se extind de la etan la distilate de vid.Folosirea etanului constituie solutia economica cea mai rationala, daca produsele ce se cer se limiteaza la etena, deoarece utilizarea care i se da etanului in cazul in care el nu este recuperat prin piroliza, este aceea de combustibil de focare.
Utilizarea etanului in piroliza presupune insa existenta unor zacaminte proprii de titei sau gaze naturale bogate din care el sa poata fi separat. Astfel de posibilitati au existat in SUA, unde etanul este folosit de mult timp pe scara larga pentru piroliza reprezentand in 1975, 39% din alimentarea instalatiilor, iar impreuna cu gazele lichefiate 75%. In Europa de Vest, pana la descoperirea zacamintelor de gaze si petrol din Marea Nodului, nu au existat surse de etan iar instalatiile de piroliza au folosit in special benzina grea. In alte tarii posesoare de resurse petroliere, in altele din Europa de Est, folosirea etanului pentru piroliza este de data mai recenta deoarece separarea lui in conditii mai rentabile din gazele de schela necesita unele utilaje de mare tehnicitate, ce nu au putut fi usor disponibile.
O situatie similara cu cea a etanului o prezinta utilizarea in piroliza a propanului si butanului, concurata insa de folosirea acestor hidrocarburi drept gaze lichefiate, ceea ce in anumite regiuni de pe glob elimina complet folosirea lor, in special a butanului pentru piroliza. Cifrele mentionate anterior pentru SUA indica importanta mare pe care o poate reprezenta in unele situatii folosirea in piroliza in special a propanului alaturi de etan. In ceea ce priveste n-butanul, trebuie mentionat ca in afara de utilizarea drept gaz lichefiat, cantitati importante sunt folosite drept adaos la benzina pentru marirea tensiunii de vapori, in special pentru a suplini cantitati insuficiente de izopentan. Cantitati mai reduse de n-butan sunt folosite pentru dehidrogenare.Asa cum s-a aratat, folosirea benzinei in piroliza s-a dezvoltat initial in tari lipsite de etan si de surse de gaze bogate, in special in Europa de Vest, obtinandu-se, alaturi de etena si propena, cantitati importante de butadiena, izopren si hidrocarburi aromatice C6 - C8, ceea ce a diminuat dezvoltarea procesele de obtinere a acestor hidrocarburi pe alte cai. Astfel, spre deosebire de SUA, in Europa de Vest nu s-aur realizat in general instalatii de fabricare a butadienei prin dehirogenarea catalitica a n-butanului, iar reformarea catalitica s-a dezvoltat in special pe linia obtinerii de benzina si nu de hidrocarburi aromatice C6 - C8.Utilizarea motorinei si in special a motorinei de vid pentru piroliza este de data mai recenta, realizarea industriala a procesului in cuptoare tubulare necesitand rezolvarea unor probleme specifice legate atat de depunerile mai importante de cocs, cat si de viteza mai mare de reactie. Odata rezolvate aceste dificultati tehnice, alegerea fractiunii lichide pirolizate a devenit o problema legata de consumul relativ de benzina sau de motorina in tara sau grupul respectiv de tari, precum si de prevederile privind evolutia acestui consum.
Astfel in SUA, unde consumul de benzina este foarte mare, dezvoltarea in continuare a pirolizei este orientata spre folosirea motorinei, in special a motorinei de vid. In alte tari, orientarea nu este de cele mai multe ori inca suficient de clara, ambele variante, piroliza benzinei sau a motorinei, fiind luate in considerare. In Romania se aprecia ca evolutia de perspectiva va fi orientata spre piroliza motorinelor, inclusiv a celor de vid, in detrimentul alegerii in acest scop a benzinei, problema care pare sa fi fost recent reluata in studiu.Trebuie mentionat ca tendinta de largire a bazei de materii prime si posibilitatile oferite de hidrotratarea prealabila a acestora, au facut sa fie luate in considerare nu numai motorinele de vid, dar chiar si uleiurile extrase din sisturile bituuminoase.In ceea ce priveste compozitia chimica a materiei prime lichide, este de mentionat necesitatea limitarii continutului de hidrocarburi aromatice si impunerea unui continut de alchene la nivelul produselor obtinute din procese primare, ambele conditii fiind legate de formarea depunerilor de cocs.
Proportiile altor clase de hidrocarburi prezente determina mai ales raportul etena/propena rezultat in efluent, n-alcanii favorizand formarea de etena iar i-alcanii si cicloalcanii pe cele de propena. In conditiile actuale, cand se urmareste obtinerea prin piroliza a unor cantitati maxime de etena.Folosirea in piroliza a unor materii prime lichide si nu a gazelor poate fi determinata si de necesitatea de a obtine alaturi de etena a altor hidrocarburi importante pentru chimizare, in special de butadiena, hidrocarburi aromatice C6 - C8 si izopren. La acestea se vor adauga cu siguranta si alte hidrocarburi pe masura rezolvarii problemelor separarii si utilizarii lor in conditii economice eficiente. Din acest punct de vedere se poate aprecia ca, utilizarea in piroliza a motorinei ofera posibilitati suplimentare inca insuficient explorate si valorificate.
Datele din tabelul urmator privind rezultatele pirolizei diverselor materii prime in conditiile obtinerii a 1000 tone etena, ofera date suplimentare, utile pentru alegerea materiei prime.
Tabel I.2. Bilantul de materiale in piroliza diverselor materii prime, raportate la 1000 t etena produsa
|
Produse |
Etan |
Propan |
Butan |
Benzina severitate |
Benzina grea severitate |
Motorina severitate |
|||
|
inalta |
medie |
inalta |
medie |
inalta |
medie |
||||
|
Gaze reziduale Etena Total fractie C3 Total fractie C4 Benzina Ulei combustibil Gaze acide |
|
|
|
|
|
|
|
|
|
|
Total |
|
|
|
|
|
|
|
|
|
|
Propena Butadiena Fractie BTX |
|
|
|
|
|
|
|
|
|
Studiul influentei materiei prime asupra procesului de cracare termica necesita cunoasterea valorilor numerice ale constantelor de viteza ale reactiilor, precum si a valorilor numerice ale energiilor de activare.
La alcanii inferiori, pana la n-pentan inclusiv, constanta vitezei de reactie creste cu cresterea masei moleculare ramanand apoi practic constanta pentru n-alcanii superiori; pentru izoalcani valoarea constantei vitezei de reactie este mai mare decat pentru n-alcani, deoarece ruperea hidrogenului de la carbonii tertiari are loc cu o viteza mai mare decat de la carbonii secundari sau primari.
Constanta vitezei de reactie creste o data cu cresterea limitelor de distilare si a factorului de caracterizare al materiei prime; ea va fi deci mai mare pentru fractiuni mai grele si pentru cele ce au un caracter alcanic (parafinos) mai pronuntat.Pentru produse de cracare, constanta de viteza este mai mica decat pentru fractiuni necracate cu aceleasi limite de distilare.
Cunoasterea variatiei valorilor constantelor de viteza si a energiei de activare in functie de caracterul chimic al materiei prime, permite sa se analizeze influenta calitatii, precum si a temperaturii din zona de reactie asupra maximului de produs intermediar.
I.5.5. Schema de principiu a instalatiei de piroliza
Intr-o instalatie de piroliza se disting doua sectii: sectia calda si sectia rece.
Materia
prima preincalzita este introdusa in partea superioara a zonei de convectie a
cuptorului. In aceasta, la un nivel de 250- 400![]() a materiei prime,
se injecteaza aburul de dilutie, iar amestecul gazos continua sa fie incalzit
pana la 550-650
a materiei prime,
se injecteaza aburul de dilutie, iar amestecul gazos continua sa fie incalzit
pana la 550-650![]() , la care este introdus in zona de radiatie. Aici prin
incalzire rapida la temperatura finala dorita se produc reactiile de piroliza.
, la care este introdus in zona de radiatie. Aici prin
incalzire rapida la temperatura finala dorita se produc reactiile de piroliza.
Pentru a opri reactiile la iesirea din cuptor, efluentul cuptorului este racit brusc in generatorul de abur de inalta presiune din care trece in coloana de fractionare calda. Aici, prin actiunea refluxurilor de recirculare si de apa, se separa gazele pe la varful coloanei, o fractie laterala de benzina si un reziduu la baza coloanei.
CAPITOLUL II
PARTEA EXPERIMENTALA
Piroliza hidrocarburilor este procesul de cracare termica la presiuni joase si temperaturi ridicate, utilizat industrial pentru fabricarea etilenei, a olefinelor si diolefinelor superioare asociate cu obtinerea ei (propilena, butilena, butadiena, izopren).
De asemenea, la piroliza fractiunilor petroliere lichide se obtin cantitati importante de hidrocarburi aromatice.
Cresterea cererilor de etilena a contribuit la extinderea gamei de materii prime de la etan la propan, butan, benzine, motorine etc., ceea ce a necesitat adaptari necorespunzatoare ale tehnologiilor de cracare a acestor materii prime si a celor de separare a componentilor la puritatea dorita. Drept materii prime se folosesc cele mai diverse fractiuni petroliere, incepand cu fractiunile gazoase si pana la reziduurile petroliere grele.
In procesul de piroliza transformarea materiei prime in produse are loc printr-un mecanism de reactii radicalice in lant, a carui cunoastere a permis, pentru anumite hidrocarburi, calculul compozitiei produselor de piroliza, cu o buna concordanta cu valorile experimentale la conversii moderate.
Viteza de transformare a materiei prime in procesele de piroliza poate fi exprimata, la conversii moderate, printr-o ecuatie cinetica de ordinul I :
![]() ,in care :
,in care :
τ este timpul de sedere, s
x este conversia materiei prime
k este constanta de viteza a reactiei, s-1
Lucrarea urmareste stabilirea influentei principalilor parametrii de operare asupra procesului (temperatura, profil de temperatura, timp de stationare in zona de reactie, raport apa/hidrocarbura), a materiei prime si a diferitelor adaosuri asupra procesului, intensitatea depunerilor de cocs pe peretele reactorului si in sistemul de racire al efluentului etc.De asemenea datele experimentale obtinute sunt folosite pentru calculul parametrilor cinetici specifici materiei prime supuse pirolizei.
Schema de principiu a instalatiei de laborator pentru piroliza benzinei este prezentata in anexa numarul 1. Reactorul tubular are de = 20 mm. Grosimea peretelui reactorului este de 3 mm iar lungimea reactorului este de 1000 mm. Distanta dintre termocuple este de 150 mm. Este confectionat din otel rezistent la temperaturi de aproximativ 1000-1200°C.
Materia prima si apa sunt trase din biuretele de alimentare (1) cu pompele dozatoare (2) si refulate prin preincalzitorul (3) in reactorul (4). Amestecul de benzina si apa circula de sus in jos prin zona de reactie iar efluentul, la iesirea din reactor, intra in racitorul de apa (5).
In separatorul de faze (6) se colecteaza fractia condensata iar gazele trec prin contorul (7) si sunt evacuate. Pot fi prelevate probe pentru analiza cromatografica fie in fiole de gaze, fie direct in fiolele cromatografului (8) legat la fluxul instalatiei.
Profilul de temperatura in lungul reactorului se inregistreaza cu ajutorul termocuplelor (9) si potentiometrului (10). Preincalzitorul (3) si reactorul (4) sunt prevazute cu incalzire electrica. Alimentarea cu energie electrica a tuturor consumatorilor se face de la tabloul electric.
Reactorul are mai multe zone de incalzire, oferind posibilitatea modificarii profilului de temperatura fie manual fie prin intermediul regulatorului de temperatura.
In functie de parametrii a caror influenta asupra procesului vrem sa o determinam se stabileste un program experimental adecvat, fixand limitele de variatie ale acestor parametri.
Incalzirea reactorului se regleaza in asa fel incat sa se obtina un profil de temperatura corespunzator pe lungimea acestuia.
Etapele de parcurs in timpul lucrarii practice sunt:
Ø
calibrarea
pompelor dozatoare de apa si materie prima (functionarea acestora cu un debit
cunoscut, apa/benzina![]()
Ø
fixarea
temperaturii (![]() 700°C) si a
timpului de lucru (15 min). Citirea temperaturii se va face din doua in doua
minute. Se inregistreaza datele obtinute conform tabelului 1. Se iau probe de
gaze pentru analiza cromatografica (Bunseng - Schilling) Colectarea probelor si
inregistrarea parametrilor de operare se face cand instalatia lucreaza in regim
stationar.
700°C) si a
timpului de lucru (15 min). Citirea temperaturii se va face din doua in doua
minute. Se inregistreaza datele obtinute conform tabelului 1. Se iau probe de
gaze pentru analiza cromatografica (Bunseng - Schilling) Colectarea probelor si
inregistrarea parametrilor de operare se face cand instalatia lucreaza in regim
stationar.
Ø principalele analize necesare prelucrarii datelor experimentale si interpretarii rezultatelor sunt: compozitia materiei prime, compozitia gazelor de piroliza, densitatea etc.
Dupa calibrare de la un volum initial de benzina de 71 cm3 se ajunge la un volum de 59 cm3 (ΔV = 12 cm 3 ) si de la un volum initial de apa de 68 cm3 se ajunge la un volum de 53 cm (ΔV=15 cm 3 ).
Tabel II.1. Profilul de temperatura
|
Citiri |
Timp, min |
T, °C |
T, K |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Densitatea benzinei
La t = 28°C :
![]() m picnometru gol = 18,9626 g
m picnometru gol = 18,9626 g
m picnometru
cu apa distilata = 44,734 g
![]() = 0,7486 g/cm3
= 0,7486 g/cm3
m picnometru cu materie prima = 38,2546 g
![]() = 0,7554 g/cm3,unde:
= 0,7554 g/cm3,unde:
dt - densitatea benzinei la temperatura de lucru, g/cm3
c- factor de corectie
m benzina =![]() benzina Vbenzina
benzina Vbenzina
m benzina = 15 · 0,7554 = 11,331 g
m apa = d apa Vapa
m apa = 15 · 1 = 15 g
S-au colectat 13 cm3 de solutie dintre care 10 cm3 apa si 3m3 produse.
Densitatea aerului umed
![]() = 0,9498 g/cm3
= 0,9498 g/cm3
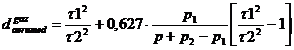 , unde :
, unde :
p - presiunea barometrica = 765 mm Hg
p1 - presiunea vaporilor de apa = 27,545 mm Hg
p2 - suprapresiunea Bunseng - Schilling =11 mm Hg
Densitatea aerului uscat
![]() = 0,9498 + 0,627 ·
= 0,9498 + 0,627 · ![]() [ 0,9498 - 1] =
0,9486 g / cm3
[ 0,9498 - 1] =
0,9486 g / cm3
daer uscat = 1,8 g/l
![]() ;
; ![]() = 0,9486 · 1,8 = 1,7075
g/cm3
= 0,9486 · 1,8 = 1,7075
g/cm3
m gaze de piroliza = 1,7075 · 5 = 8,5375 g
Se verifica bilantul material :
I : benzina = 11,331 g 43,03%
apa = 15 g 56,97%
TOTAL = 26,331g
E : m benzina de piroliza = 1,5108 g 5,73%
m gaze de piroliza = 8,53 g 32,42%
m apa = 15 g 56,97%
TOTAL = 25,0483
(pierderi + cocs) = 26,331 - 25,0483 = 1,2827 g 4,87%
Tabel II.2. Distributia cromatografica a produsilor de reactie
|
Produs |
Fractie molara, Xi |
Masa molara, kg/kmol |
|
CH4 |
48,42 |
|
|
C2H6 |
7,81 |
|
|
C2H4 |
36,19 |
|
|
C3H8 |
1,27 |
|
|
C4H10 |
11,82 |
|
|
1-C4H8 |
|
|
|
2- C4H8 |
|
|
![]() = 29,027 kg / kmol
= 29,027 kg / kmol
Pentru prelucrarea datelor se cunosc:
dreactor = 2 cm
distanta intre termocuple = 15 cm
ΔV = 47,124 cm3
R = 1,98 cal/ mol K
E = 65000 cal/mol
a) Treactie = 973 K
|
ΔV, cm3 |
T, K |
F= |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Vreactie = ΔV ( ![]() ) = 47,124 ( 0,00008 + 1,20621 ) = 56,845cm3
) = 47,124 ( 0,00008 + 1,20621 ) = 56,845cm3
τechiv
= ![]()
Vmed =![]()
Vi =![]() unde :
unde :
ni - numarul de moli de materie prima
R - constanta gazelor, atm m3 / kmol K
Ti - temperatura la intrarea in reactor, K
pi - presiunea la iesirea din reactor, atm.
ni =![]() = 0,936
= 0,936
Vi =![]() = 39,39 l/ 15 min
= 39,39 l/ 15 min
Ve = ![]()
ne =![]() =
=![]()
Ve = ![]() = 72,32 l/ 15 min.
= 72,32 l/ 15 min.
Vmed = ![]() = 55,86 l / 15 min.
= 55,86 l / 15 min.
Vmed = ![]() = 0,062 l/s = 62
cm3/s
= 0,062 l/s = 62
cm3/s
τechiv
= ![]() = 0,92 s
= 0,92 s
k =![]() = 0,426 s-1
= 0,426 s-1
lnk = -0,853
1/ Treactie = 0,001027
b) Treactie = 993 K
|
ΔV, cm3 |
T, K |
F= |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Vreactie = ΔV ( ![]() ) = 47,124 ( 0,0000411 + 0,101895 ) = 28,81 cm3
) = 47,124 ( 0,0000411 + 0,101895 ) = 28,81 cm3
τechiv
=![]()
τechiv
= ![]() = 0,4647s
= 0,4647s
k =![]() = 0,843 s-1
= 0,843 s-1
lnk = -0,17
1/ Treactie = 0,001007
c )Treactie = 953 K
|
ΔV, cm3 |
T, K |
F= |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Vreactie = ΔV (![]() ) = 47,124 ( 0,000165 + 0,408133 ) = 115,399 cm3
) = 47,124 ( 0,000165 + 0,408133 ) = 115,399 cm3
τechiv
= ![]()
τechiv
=![]() = 1,86 s
= 1,86 s
k =![]() = 0,21 s-1
= 0,21 s-1
lnk = -1,557
1/ Treactie = 0,001049
In urma calculului efectuat se va trasa grafic variatia temperaturii cu constanta de viteza, k, grafic ce va fi folosit in partea de calcul tehnologic pentru citirea lui k si stabilirea temperaturii de iesire din zona de radiatie a cuptorului
CAPITOLUL III
CALCULUL TEHNOLOGIC
Capacitatea sectiei de reactie a cuptorului : 90 000 t
Natura materiei prime : Propan
Compozitie : 98,2% C3H8
0,4% C2H6
1,4% C4H10
Temperatura de intrare in cuptor, tic = 100°C
Presiunea de intrare in cuptor, pic = 5,5 atm
Temperatura de incepere a reactiilor, tir = 650°C
Raportul apa / materie prima, a = 0,6 kg/kg
Distributia produsilor de reactie la iesirea din cuptor:
Tabel III.1. Distributia produsilor de reactie la iesirea din cuptor
|
Component |
% gr |
|
H2 |
|
|
CH4 |
|
|
C2H2 |
|
|
C2H4 |
|
|
C2H6 |
|
|
C3H6 |
|
|
C3H8 |
|
|
C4H6 |
|
|
C4H8 |
|
|
C4H10 |
|
|
C5 |
|
Tensiunea termica in zona de convectie, Φtc = 25000 kmol/ m2 h
Tensiunea termica in zona de radiatie, Φtr = 75000 kmol/ m2 h
Date constructive ale tuburilor din cuptor:
diametrul interior, Di = 0,1 m
diametrul exterior, De = 0,12 m
lungimea tuburilor, l = 8 m
Conversia globala pe reactor, x = 92 %
Numarul de ore de functionare, N = 7680
Sarcina maxima a serpentinei ( materie prima + abur ) = 2500 kg/ h
Pentru stabilirea modelului matematic se fac urmatoarele presupuneri:
Reactia de piroliza are loc in zona de radiatie a cuptorului, iar zona de convectie constituie zona de incalzire si vaporizare a materiei prime pana la temperatura de inceput a reactiilor, tir.
Pentru calculul serpentinei se considera ca aceasta este impartita in sectoare de lungime suficient de mica astfel incat conversia realizata in fiecare sector sa fie mai mica putandu-se calcula astfel valorile medii ale temperaturii, numarul de moli, presiunea la intrarea si iesirea din sector.
Pentru fiecare sector se fac presupuneri ale valorii temperaturii, presiunii si conversiei urmand ca ele sa fie verificate cu o marja de eroare care sa nu depaseasca 5%.
Calculul numarului de serpentine
Numarul de serpentine trebuie sa fie intreg si par.
![]()
![]() ns =
ns = ![]()
![]()
unde:
ns - numarul de serpentine
Gmp - debitul de materie prima, kg/h
Gabur - debitul de abur, kg/h
Gmp = 90 000 · ![]() 11718,75 kg/h
11718,75 kg/h
Gabur = a · Gmp
Gabur = 0,6 · 11718,75 = 7031,25 kg/h
ns = ![]()
ns= 8
Gmp pt o serpentina = ![]() =
= ![]() = 1464,84 kg/h
= 1464,84 kg/h
Gabur pt o serpentina = ![]() =
= ![]() = 878,9 kg/h
= 878,9 kg/h
Se verifica relatia:
(Gmp + Gab) serpentina ≤ Smax
2343,75≤ 2500 (adevarat)
Pentru dimensionarea serpentinei cuptorului se va incepe cu sectia de convectie, aici se va determina lungimea serpentinei si caderea de presiune.
In acest scop se va folosi bilantul termic.
Serpentina va fi impartita in cinci zone, astfel:
C 200 C 300 C 400 C 500 C 650 C
![]() Zona I Zona II Zona
III Zona IV Zona V
Zona I Zona II Zona
III Zona IV Zona V
III.3.1. Calculul sectorului I
100ºC 200ºC
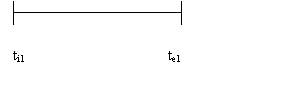 Sectorul
I
Sectorul
I
unde:
ti - temperatura de intrare in sector, °C
te - temperatura la iesirea din sector, °C
tm - temperatura medie
![]()
![]()
tm=![]()
![]()
![]()
![]()
![]() unde :
unde :
pe1 - presiunea la iesirea din sectorul I, atm.
![]() - masa molara
medie, kmol/kg
- masa molara
medie, kmol/kg
R - constanta gazelor ideale = 0,08
T - temperatura, K
![]()
![]()
![]()
![]()
![]()
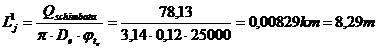
Qsch - caldura schimbata, kcal/h
De - diametrul exterior al tuburilor, m
φtc - tensiunea termica in zona de convectie, kmol/ m2 · h
Lungimea echivalenta se calculeaza astfel:
![]()
Caderea de presiune se calculeaza dupa relatia:
![]()
![]()
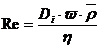
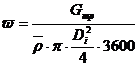 , unde:
, unde:
w - viteza de reactie, m/s
![]() - densitatea
medie, kg/m3
- densitatea
medie, kg/m3
di - diametrul interior al tuburilor, m
Gmp I - debitul de materie prima pe o serpentina, kg/h
![]()
![]()
Calculul masei molare medii a gazelor
![]()
![]()
![]()
![]()
![]()
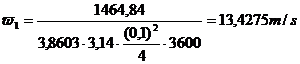
![]()
![]()
![]()
![]() μ - vascozitatea cinematica, P
μ - vascozitatea cinematica, P
![]()
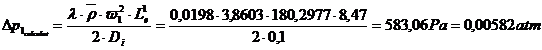
![]()
Eroarea se va calcula dupa relatia:
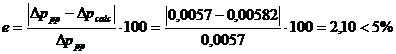
III.3.2. Calculul sectorului II:
![]() 200ºC Sectorul II 300ºC
200ºC Sectorul II 300ºC
ti2 te2
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
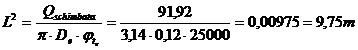
![]()
![]()
![]()
![]()
![]()
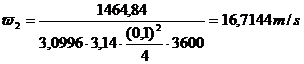
![]()
![]()
![]()
![]()
![]()
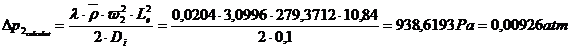
![]()
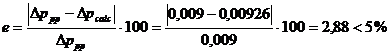
III.3.3. Calculul sectorului III
300ºC
400ºC
![]() Sectorul III
Sectorul III
ti3 te3
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
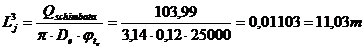
![]()
![]()
![]()
![]()
![]()
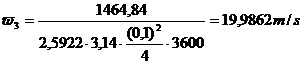
![]()
![]()
![]()
![]()
![]()
![]()
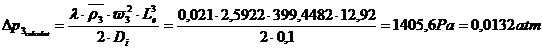
![]()
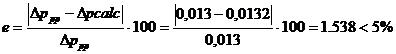
III.3.4. Calculul sectorului IV
ti4 te4 Sectorul IV
C 500 C
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
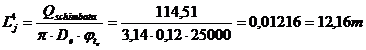
![]()
![]()
![]()
![]()
![]()
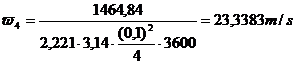
![]()
![]()
![]()
![]()
![]()
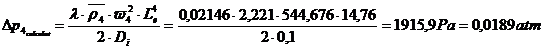
![]()
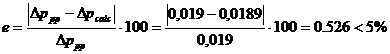
III.3.5. Calculul sectorului V
Sectorul V
![]()
ti5
te5
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
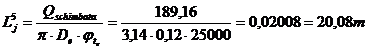
![]()
![]()
![]()
![]()
![]()
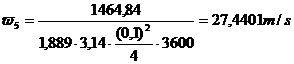
![]()
![]()
![]()
![]()
![]()
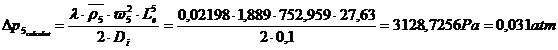
![]()
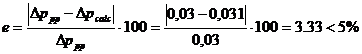
Tabel III.2.
|
Comp |
gir % gr |
gip % gr |
Mir kg/kmol |
Mip kg/kmol |
nir moli/100g |
nip moli/100g |
ΔHf kcal/mol |
nip · ΔHf kcal/100g |
nir · ΔHf kcal/100g |
|
H2 |
|
|
|
|
|
|
|
|
|
|
CH4 |
|
|
|
|
|
|
|
|
|
|
C2H2 |
|
|
|
|
|
|
|
|
|
|
C2H4 |
|
|
|
|
|
|
|
|
|
|
C2H6 |
|
|
|
|
|
|
|
|
|
|
C3H6 |
|
|
|
|
|
|
|
|
|
|
C3H8 |
|
|
|
|
|
|
|
|
|
|
C4H6 |
|
|
|
|
|
|
|
|
|
|
C4H8 |
|
|
|
|
|
|
|
|
|
|
C4H10 |
|
|
|
|
|
|
|
|
|
|
C5+ |
|
|
|
|
|
|
|
|
|
|
TOTAL |
|
|
|
|
|
|
|
|
|
Ca si la zona de convectie, zona de radiatie se va imparti in sectoare pe fiecare sector calculandu-se caderea de presiune,lungimea serpentinei si conversia.
Zona de radiatie va fi impartita in 3 sectoare:
![]()
![]()
![]()
![]()
![]() 650°C 700°C 750°C 800oC
650°C 700°C 750°C 800oC
III.4.1. Calculul sectorului I
C 700 C
Sectorul I ti1 te1
![]()
![]()
![]()
![]()
Se presupune: ![]()
![]()
Se presupune: ![]()
pi1 - presiunea la intrarea in sector, atm.
pe - presiunea la iesirea din sector, atm
Δx1 - conversia pe sectorul I
BT: 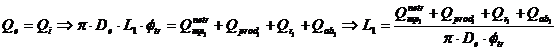 unde:
unde:
![]() debitul caloric de materie prima netransformata, kcal/h;
debitul caloric de materie prima netransformata, kcal/h;
![]() debitul caloric de produsi rezultati, kcal/h;
debitul caloric de produsi rezultati, kcal/h;
![]() debitul caloric al reactiei, kcal/h;
debitul caloric al reactiei, kcal/h;
![]() debitul caloric de abur adaugat in sistem, kcal/h;
debitul caloric de abur adaugat in sistem, kcal/h;
Hr - entalpia de reactie, kcal/kg
![]()
![]()
![]()
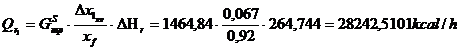
Singurele
produse rezultate sunt gazele,deci:![]()
![]() ,unde:
,unde:
![]() fractia molara de gaze rezultate din primul sector;
fractia molara de gaze rezultate din primul sector;
![]() entalpia gazelor la temperatura medie, kcal/kg;
entalpia gazelor la temperatura medie, kcal/kg;
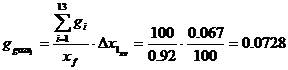
![]()
![]()
![]()
![]()
![]()
Hte - entalpia materiei prime netransformate la iesirea din sector, kcal/kg
Hti - entalpia materiei prime la intrarea in sector, kcal/kg
![]()
Ite , Iti - entalpiile aburului la intrarea si iesirea din sector, kcal/kg
Din literatura se cunoaste ca:
![]()
![]()
![]()
![]()
![]()
Le1 = (n-1) · 50 ·Di + L1 =7,30 m
Se efectueaza verificarea bilantului masic:
1358,2 kg/h 106,6 kg/h 878,9 kg/h 2343,74 kg/h
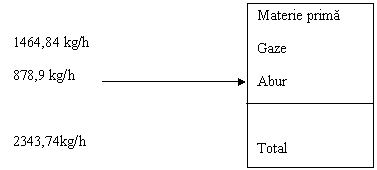

Se verifica atat conversia cat si caderea de presiune:
Masa moleculara la intrarea in sector:
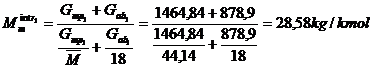
Masa moleculara la iesirea din sector:
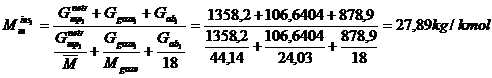
Densitatea vaporilor la intrarea si iesirea din sector:
![]()
![]()
![]()
Viteza vaporilor in sectorul I:
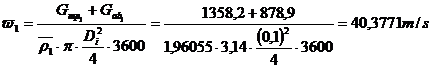
![]()
Vascozitatea se determina cu ajutorul formulei:
![]() ,unde:
,unde:
![]() reprezinta vascozitatea critica; kg/ m · s
reprezinta vascozitatea critica; kg/ m · s
![]() reprezinta vascozitatea redusa, se determina din graficul 2.2.25
[4] ,kg/ m · s
reprezinta vascozitatea redusa, se determina din graficul 2.2.25
[4] ,kg/ m · s
Vascozitatea critica se determina cu formula:
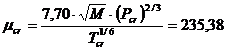 kg/ m · s
kg/ m · s
Din literatura se cunoaste:
![]() presiunea critica a propanului = 43,3 atm;
presiunea critica a propanului = 43,3 atm;
![]() temperatura critica a propanului = 369,95K;
temperatura critica a propanului = 369,95K;
Pentru determinarea vascozitatii este necesar cunoasterea presiunii si a temperaturii reduse, acestea se afla astfel:
![]()
![]()
Cu ajutorul temperaturii reduse si presiunii reduse se va citi μred , si apoi se va determina μ la temperatura dorita.
![]() . kg/ m · s
. kg/ m · s
λ = 0,16 · Re-0,16
![]()
Calculul caderii de presiune in sectorul I:
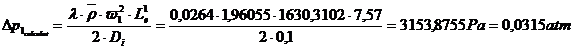
![]()
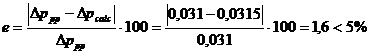
b. Verificarea conversiei
![]() ,unde:
,unde:
![]() volumul zonei de radiatie a sectorului unu.
volumul zonei de radiatie a sectorului unu.
Numarul de moli de materie prima la intrarea in sector:
![]()
Numarul de moli de produse la iesirea din sector:
![]()
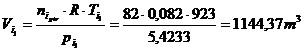
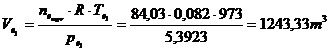
![]()
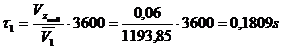
![]()
![]()
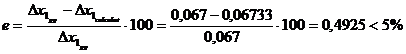
III.4.2. Calculul sectorului II
Sectorul II
![]()
|
![]()
![]()
![]()
![]()
Se presupune: ![]()
![]()
Se presupune: ![]()
BT: ![]()
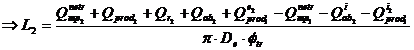 ,unde:
,unde:
![]() debitul caloric de materie prima netransformata la iesirea
din cel de-al doilea sector, kcal/h;
debitul caloric de materie prima netransformata la iesirea
din cel de-al doilea sector, kcal/h;
![]() debitul caloric de produsi rezultati din cel de-al doilea
sector, kcal/h;
debitul caloric de produsi rezultati din cel de-al doilea
sector, kcal/h;
![]() debitul caloric al reactiei din sectorul doi, kcal/h;
debitul caloric al reactiei din sectorul doi, kcal/h;
![]() debitul caloric de abur adaugat la iesirea din sectorul doi,
kcal/h;
debitul caloric de abur adaugat la iesirea din sectorul doi,
kcal/h;
![]() debitul caloric de produsi rezultati din primul sector la
iesirea din sectorul doi, kcal/h;
debitul caloric de produsi rezultati din primul sector la
iesirea din sectorul doi, kcal/h;
![]() debitul caloric de
materie prima netransformata din primul sector, kcal/h;
debitul caloric de
materie prima netransformata din primul sector, kcal/h;
![]() debitul caloric de
abur adaugat la intrarea in sectorul doi, kcal/h;
debitul caloric de
abur adaugat la intrarea in sectorul doi, kcal/h;
![]() debitul caloric de
produsi rezultati din primul sector la intrarea in sectorul doi, kcal/h;
debitul caloric de
produsi rezultati din primul sector la intrarea in sectorul doi, kcal/h;
![]()
![]()
![]()
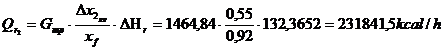
Singurele
produse rezultate sunt gazele,deci:![]()
![]() ,unde:
,unde:
![]() fractia molara de gaze rezultate din cel de-al doilea sector;
fractia molara de gaze rezultate din cel de-al doilea sector;
![]() entalpia gazelor la temperatura medie, kcal/kg;
entalpia gazelor la temperatura medie, kcal/kg;
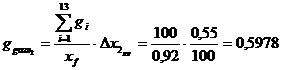
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Din literatura se cunoaste ca:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
546,268 kg/h 106,6404 kg/h 811,932 kg/h 878,9 kg/h 2343,74 kg/h
 Se efectueaza
verificarea bilantului masic:
Se efectueaza
verificarea bilantului masic:

Se verifica atat conversia cat si caderea de presiune:
a. Verificarea caderii de presiune
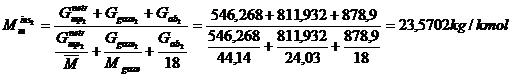
![]()
![]()
![]()
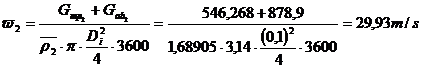
![]()
Vascozitatea se determina cu ajutorul formulei:
![]() ,unde:
,unde:
![]() reprezinta vascozitatea critica; kg/m·s
reprezinta vascozitatea critica; kg/m·s
Vascozitatea critica se determina cu formula:
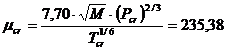 kg/m·s
kg/m·s
Din literatura se cunoaste:
![]() presiunea critica a propanului = 43,3 atm;
presiunea critica a propanului = 43,3 atm;
![]() temperatura critica a propanului = 369,95 K;
temperatura critica a propanului = 369,95 K;
Pentru determinarea vascozitatii este necesar cunoasterea presiunii si a temperaturii reduse, acestea se afla astfel:
![]()
![]()
![]() . kg/m·s
. kg/m·s
![]() kg/m·s
kg/m·s
![]()
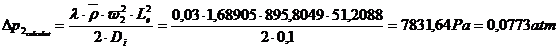
![]()
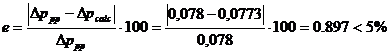
b. Verificarea conversiei
![]() ,unde:
,unde:
![]() volumul zonei de radiatie a sectorului doi.
volumul zonei de radiatie a sectorului doi.
![]()
![]()
![]()
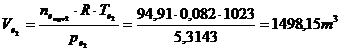
![]()
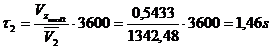
![]()
![]()
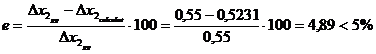
III.4.3. Calculul sectorului III
![]() 750ºC Sectorul III 800ºC
750ºC Sectorul III 800ºC
ti3 te3
![]()
![]()
![]()
![]()
Se presupune:
![]()
![]()
Conversia
este: ![]()
BT: ![]()
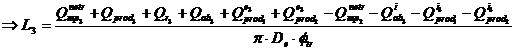 ,unde:
,unde:
![]() debitul caloric de materie prima netransformata la iesirea
din cel de-al treilea sector, kcal/h;
debitul caloric de materie prima netransformata la iesirea
din cel de-al treilea sector, kcal/h;
![]() debitul caloric de produsi rezultati din cel de-al treilea
sector, kcal/h;
debitul caloric de produsi rezultati din cel de-al treilea
sector, kcal/h;
![]() debitul caloric al reactiei din sectorul trei, kcal/h;
debitul caloric al reactiei din sectorul trei, kcal/h;
![]() debitul caloric de abur la iesirea din sectorul trei, kcal/h;
debitul caloric de abur la iesirea din sectorul trei, kcal/h;
![]() debitul caloric de produsi rezultati din primul sector la
iesirea din sectorul trei, kcal/h;
debitul caloric de produsi rezultati din primul sector la
iesirea din sectorul trei, kcal/h;
![]() debitul caloric de
produsi rezultati din sector doi la iesirea din sectorul trei, kcal/h;
debitul caloric de
produsi rezultati din sector doi la iesirea din sectorul trei, kcal/h;
![]() debitul caloric de
materie prima netransformata din sectorul doi, kcal/h;
debitul caloric de
materie prima netransformata din sectorul doi, kcal/h;
![]() debitul caloric de
abur adaugat la intrarea in sectorul trei, kcal/h;
debitul caloric de
abur adaugat la intrarea in sectorul trei, kcal/h;
![]() debitul caloric de
produsi rezultati din primul sector la intrarea in sectorul trei, kcal/h;
debitul caloric de
produsi rezultati din primul sector la intrarea in sectorul trei, kcal/h;
![]() debitul caloric de
produsi rezultati din sector doi la intrarea in sectorul trei, kcal/h.
debitul caloric de
produsi rezultati din sector doi la intrarea in sectorul trei, kcal/h.
![]()
![]()
![]()
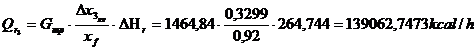
Singurele produse rezultate sunt gazele,deci:![]()
![]() ,unde:
,unde:
![]() fractia molara de gaze rezultate din cel de-al treilea
sector;
fractia molara de gaze rezultate din cel de-al treilea
sector;
![]() entalpia gazelor la temperatura medie, kcal/kg;
entalpia gazelor la temperatura medie, kcal/kg;
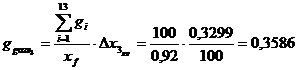
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Din literatura se cunoaste ca:
![]()
![]()
![]()
![]()
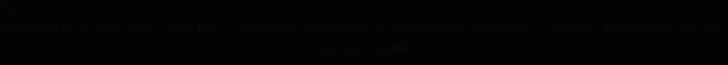
![]()
![]()
Se efectueaza verificarea bilantului masic:
546,268 kg/h 106,6404 kg/h 811,932 kg/h 878,9 kg/h 2343,74 kg/h 350,378 kg/h 106,6404 kg/h 811,932 kg/h 195,89 kg/h 878,9 kg/h 2343,74 kg/h


![]()
Se verifica atat conversia cat si caderea de presiune:
a. Verificarea caderii de presiune
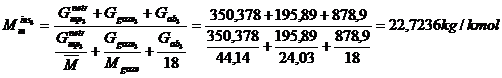
![]()
![]()
![]()
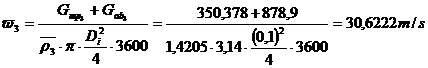
![]()
Vascozitatea se determina cu ajutorul formulei:
![]() ,unde:
,unde:
![]() reprezinta vascozitatea critica; kg/m·s
reprezinta vascozitatea critica; kg/m·s
![]() reprezinta vascozitatea redusa, kg/m·s
reprezinta vascozitatea redusa, kg/m·s
Vascozitatea critica se determina cu formula:
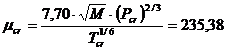 kg/m·s
kg/m·s
Din literatura se cunoaste:
![]() presiunea critica a propanului = 43,3atm;
presiunea critica a propanului = 43,3atm;
![]() temperatura critica a propanului = 369,95 K;
temperatura critica a propanului = 369,95 K;
Pentru determinarea vascozitatii este necesar cunoasterea presiunii si a temperaturii reduse, acestea se afla astfel:
![]()
![]()
![]() . kg/m·s
. kg/m·s
![]() kg/m·s
kg/m·s
![]()
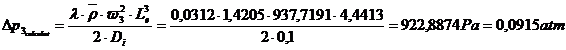
![]()
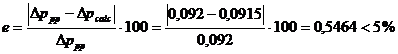
b. Verificarea conversiei
![]() ,unde:
,unde:
![]() volumul zonei de radiatie a sectorului trei.
volumul zonei de radiatie a sectorului trei.
![]()
![]()
![]()
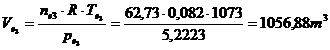
![]()
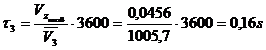
![]()
![]()
k3 (citit din graficul de la partea experimentala, la temperatura presupusa de 800°C ) = 2,05
![]() 2,05·0,16=0,328
2,05·0,16=0,328
e=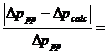
![]() =0.18 ≤ 5%
=0.18 ≤ 5%
CONCLUZII:
Pentru zona de convectie si sectoarele I si II din radiatie, caderea de presiune si conversia s-au determinat prin presupuneri repetate, iar temperatura la iesire din zona de radiatie s-a determinat deasemenea prin presupuneri repetate;
Timpul de reactie rezultat este τ = 2,1 s
Numarul de serpentine si lungimea acestora din cele doua zone ale cuptorului sunt apropiate de cele reale;
Zona de convectie
|
|
Ti, °C |
Te , °C |
ΔP, atm |
L, m |
Lech |
|
Sector I |
|
|
|
|
|
|
Sector II |
|
|
|
|
|
|
Sector III |
|
|
|
|
|
|
Sector IV |
|
|
|
|
|
|
Sector V |
|
|
|
|
|
|
TOTAL |
|
|
|
|
|
Zona de radiatie
|
|
Ti, °C |
Te , °C |
ΔP, atm |
L, m |
Lech |
ΔX |
|
Sector I |
|
|
|
|
|
|
|
Sector II |
|
|
|
|
|
|
|
Sector III |
|
|
|
|
|
|
|
TOTAL |
|
|
|
|
|
|
CAPITOLUL IV
CALCULUL ECONOMIC
Prin acest capitol s-a urmarit estimarea eficientei economice a unei instalatii de piroliza. Calculele economice de rentabilitate trebuie sa tina seama de pretul materiilor prime si al produselor finite la data intrarii in functiune a instalatiei.
Profitul realizat de o intreprindere pentru o anume instalatie se reprezinta prin diferenta dintre valoarea produselor obtinute si cheltuielile de productie.
PROFIT = VALOARE PRODUS - CHELTUIELI
![]()
Cheltuielile de productie (CP) se estimeaza prin insumarea cheltuielilor directe (CD) si a cheltuielilor indirecte (CI).
![]()
![]()
C1 = cheltuieli cu materia prima;
C2 = cheltuieli cu energia si materiale auxiliare utilizate in instalatie si utilitati;
C3 = costul energiei recuperate si refolosite ( C3 = 0);
C4 = fond de retribuire ( salarizare) directa;
C5 = A = amortizarea fondurilor fixe.
![]()
C6 = cheltuieli pentru intretinere ai reparatii;
C7 = cheltuieli generale efectuate la nivelul unitatii;
C8 = fond retributii indirecte;
C9 = cheltuieli pentru asigurari sociale ( CAS );
C10 = cheltuieli cu PM si PSI;
C11 = cheltuieli pentru pompari, depozitari, livrari;
C12 = cheltuieli desfacere.
Indicatori de utilizare a instalatiei
![]()
Tp = timp productiv (functionare), 7 680 h/an
Tc = timp calendaristic = 365 · 24 = 8 760
Timp de oprire revizie generala = 30 zile/an
D = capacitatea de productie : 90000 t/an
Materie prima : propan
|
Supus prelucrarii |
Randament, % |
Cantitate, t/an |
Pret, lei/t |
Valoare, lei/an |
|
Propan |
|
|
|
C1 = 1,8 |
Tabel IV.1. Calculul cheltuielilor cu materia prima (C1 )
![]()
![]()
![]()
Cheltuielile cu salariile directe cuprind toate veniturile (salarii, ore suplimentare, prime, ajutoare) pentru personalul operator al instalatiei.
Calculul salariilor directe s-a facut avand la baza negocierea scrisa intre patronat si sindicate luand in calcul salariu mediu.
C4 = total personal · retributie lunara · 12 luni
![]()
![]()
It = investitie totala = 4,2 · 107 lei/an
Dns = durata normala de serviciu = 20 ani
![]()
Calculul cheltuielilor directe
![]()
![]()
Cheltuieli indirecte: salarii generale de conducere, CAS-ul, ajutorul de somaj aferent, cota de amortizare pentru fonduri fixe ale administratiei, cheltuieli administrativ gospodaresti ( deplasari-delegatii, cheltuieli telefon, fax, telex, impozite si taxe, dobanzi).
![]()
![]()
Pentru instalatia de piroliza pentru C7 se aplica o cota de 20% din cheltuieli directe.
![]()
Aceste categorii de cheltuieli (indirecte) cuprind: amortizarea, reparatiile si reviziile programate de primavara si iarna efectuate cu forte proprii si terti, cheltuieli de protectia muncii si unele cheltuieli indirecte efectuate la nivel de societate privind protectia mediului, cercetare-dezvoltare.
![]()
C9 = CAS = reprezinta conform legii in vigoare 10% din salariile directe.
![]()
Ajutorul de somaj reprezinta 0,5% din salariile directe. Astfel :
![]()
C10 = cheltuieli cu PM si PSI in instalatie pentru salariati si cheltuieli cu protectia mediului.
![]()
![]()
![]()
![]()
![]()
Calculul cheltuielilor indirecte
![]()
![]()
![]()
![]()
Tabel IV.2. Calculul profitului (beneficiu)
|
Produs |
Randament |
Cantitate |
Pret , lei/t |
Valoare , lei/an |
|
H2 |
|
|
|
|
|
CH4 |
|
|
|
8 8,88 |
|
C2H4 |
|
|
|
|
|
C2H6 |
|
|
|
|
|
C3H6 |
|
|
|
|
|
C3H8 |
|
|
|
|
|
C5+ |
|
|
|
|
|
Total |
|
|
|
V = 3,37 |
![]()
![]()
Rp = rata profitului
![]()
Rp = reprezinta beneficiul real realizat de instalatia de piroliza a propanului.
a) Investitia specifica:
![]()
b) Cheltuieli de prelucrare pe tona de materie prima
![]()
c) Valorificarea tonei de materie prima
![]()
d) Indicatorul de valorificare a materiei prime :
![]()
![]()
CAPITOLUL V
NORME DE PROTECTIA MUNCII
IN INSTALATIILE DE PIROLIZA
V. NORME DE PROTECTIA MUNCII SI MEDIULUI
In instalatiile de cracare termica, pericolul de avarii si incendii este mai mare decat in instalatiile de distilare primara a titeiului si in cele de distilare secundara a pacurii, datorita temperaturilor si uneori a presiunilor mai mari.
Se impune asadar respectarea cu strictete a urmatoarelor norme:
se impune folosirea echipamentului de lucru la locurile de munca;
este interzis lucrul cu foc deschis in perimetrul in stalatiei;
este obligatorie izolarea si ermetizarea vaselor de lucru;
este necesara legarea la pamant a utilajelor care acumuleaza energie statica;
se interzice folosirea pompelor necorespunzatoare conditiilor tehnice de temperatura si presiune a produsului pompat.
se interzice folosirea aparaturii fara a controla presiunea in aceasta.
se interzice folosirea coturilor de intoarcere defecte, care au scapari de produse, precum si deschiderea acestora in timpul functionarii cuptorului.
se interzice folosirea temperaturii peste 100°C in partea inferioara a coloanei de fractionare fara golirea prealabila a apei.
se interzice a se lucra cu scapari de produse la conducte si robinete.
se interzice pornirea instalatiei daca instalatia de stingere cu abur nu e in buna stare, daca supapele de siguranta de la aparate sunt defecte si fara a asigura conducta de golire rapida a instalatiei. Toate lucrarile de reparatii pe teritoriul instalatiei cu mediu de gaze inflamabile trebuie sa se execute cu scule care nu produc scantei (bronz, alama). Incalzirea liniilor tehnologice inghetate, pe timp de iarna se va face numai cu abur sau apa. Se interzice fortarea deschiderii cu carligul, a robinetelor inghetate sau blocate de produse congelate.
se vor utiliza si monta garnituri corespunzatoare regimului de functionare dupa cum urmeaza: garnituri din carton presat pentru conducte de apa; garnituri din clingherit pentru conducte de abur si produse care functioneaza la presiuni pana la 20 daN/cm2 si la temperaturi pana la 65°C sau pana la presiuni de 10 daN/cm2 si temperaturi de 300°C; garnituri din tabla de aluminiu umplute cu azbest de calitate pentru conducte cu presiunea pana la 20 daN/cm2 si temperaturi pana la 65°C sau pana la presiuni de 10 daN/cm2 si temperaturi de 400°C;
la vasele si conductele care contin produse sub presiune ridicata, fierbinti sau gaze lichefiate, se interzice desfacerea legaturilor de scurgere, pentru a incerca desfundarea lor. De asemenea se interzice desfundarea acestor legaturi cu sarma prin ventil sau prin lovire. Desfundarea lor se va face prin presiune cu abur, in care scop se vor prevedea legaturi speciale la instalatia respectiva.
Pentru prevenirea accidentelor se iau urmatoarele masuri:
- instruirea corespunzatoare a personalului operativ;
- blindarea conductelor de gaze, aerisirea cuptorului dupa intreruperea gazelor, aburirea spa-tiilor de ardere;
- scurgerea completa a apei din aparat, izolarea completa a schimbatorului, scurgerea apei din conducte inainte de punerea in functiune;
- golirea si aburirea completa a aparatului.
Pentru a evita crearea conditiilor favorabile in care se pot produce incendiile la rezervoare, este ne-cesara luarea unor masuri care sa duca la:
- asigurarea etanseitatii perfecte a instalatiilor si a rezervoarelor la capace si manta pentru a impiedica iesirea vaporilor si a amestecului aer-vapori in acest mod necontrolat si raspandirea lor in atmosfera;
- echiparea rezervoarelor la gurile de aerisire cu opritoare, exploatarea fara greseli de opera-re a instalatiilor tehnologice si a rezervoarelor;
- eliminarea imediata a tuturor defectiunilor care apar in cursul exploatarii si care ar putea deveni surse de incendiu;
- prin destinderea hidrocarburilor usoare se pot produce in utilajul respectiv temperaturi mai mici decit temperatura maxima admisibila de lucru pentru care acesta a fost calculat. Daca un utilaj a fost racit sub aceasta temperatura inainte de evacuarea lichidului se va evita aducerea rapida a uti-lajului rece si eventual casant la presiunea initiala sau supunerea la socuri.
Personalul care deserveste instalatia trebuie sa fie instruit pentru a respecta normele de teh-nica securitii nuncii, fiind necesara verificarea cunostintelor periodic, pentru a asigura o disciplina de munca corespunzatoare.
Instalatiile
de piroliza a hidrocarburilor sunt de o complexitate deosebita incluzind etape
de reactie la temperaturi ridicate de racire prin contact direct cu apa, ![]() de fractionare, de vehiculare gaze, de
uscare gaze etc.
de fractionare, de vehiculare gaze, de
uscare gaze etc.
In procesul de piroliza pe langa compusii principali valorosi, etena si propena, se formeaza in reactii secundare compusi nesaturati (olefine, diene, hidrocarburi aromatice).
Prin reactii de condensare se formeaza cantitati variabile de asa numita benzina de piroliza si de reziduu de piroliza. Asa cum arata literatura de specialitate unii din compusii benzinei si rezi-duurile de piroliza sunt de o toxicitate variabila de la mediu la foarte toxic.
De mentionat ca prezenta in cantitati foarte mici a hidrocarburilor policiclice aromatice de tipul benzopirenului la contactul cu tesuturile vii declanseaza cancer.
In consecinta, instalatia de piroliza trebuie bine izolata de contactul cu solul printr-un plan- seu de beton continuu pentru a se impiedica accesul la panza freatica. Trebuie sa se acorde o atentie deosebita etansarilor de diverse tipuri (pe conducte, la pompe, la compresoare s.a.).
Sunt necesare inspectii atente si periodice pentru depistarea la timp a unor eventuale defectiuni, cum ar fi fisurari: de serpentina in cuptor, la generatorul de abur, la coloana de spalare cu apa etc. Personalul care opereaza in instalatie trebuie echipat cu masti cu filtre dispuse pe nas si pe gura, manusi de cauciuc si salopeta cauciucata atunci cand accesul este in zone ale instalatiei cu posibil contact cu benzina si reziduu de piroliza.
Platforma trebuie prevazuta cu canale si colectoare de fractii petroliere dirijate spre canale colectoare, conducand la statia de epurare chimica si biologica.
Rezervoarele si vasele in care se vehiculeaza benzina si reziduul de piroliza trebuiesc prevazute cu dispozitive care sa impiedice respiratia in atmosfera.
In cadrul reviziilor si a perioadelor de decocsare a cuptoarelor si a zonei calde (regeneratoarele de abur) se vor lua masuri pentru protejarea personalului de revizie impiedicandu-se degajarea in tim-pul damfuirii a traseelor de vapori de produsi de reactie depusi si absorbiti pe peretii interiori ai sectiei calde.
Cocsul format la piroliza contine in compozitia sa pe langa un material cu continut ridicat de carbon si compusi intermediari ai cocsului de tipul hidrocarburilor aromatice policiclice cu actiune toxico-fiziologica mentionata mai sus. De asemenea in sectorul de vehiculare si depozitare a benzinei si reziduului de piroliza revi- ziile si interventiile se vor face cu un personal instruit si echipat astfel incat sa fie protejat de contactul, prin respiratie si prin piele, de produsii cu actiune toxica.
Raseev, S., - Conversia hidrocarburilor, vol I, Ed. Zecasin, Bucuresti 1994
Vantu, V., Mihail R., Macris V., - Piroliza hidrocarburilor, Ed. Tehnica, Bucuresti 1980
Suciu, Gh., - Ingineria prelucrarii hidrocarburilor, vol IV, Ed. Tehnica, Bucuresti 1993
Suciu, Gh., Tunescu, R., - Ingineria prelucrarii hidrocarburilor, vol I, Ed. Tehnica, Bucuresti 1983
Suciu, G., Tunescu, R., - Ingineria prelucrarii hidrocarburilor, vol II, Ed. Tehnica, Bucuresti 1974
Ionescu, C., Dumitrascu, G., Rosca, P., Onutu, I., - Procese termocatalitice (indrumar de laborator), Ed. UPG, Ploiesti 1985
Rossini, F.D., - Selected values of physical and termodynamic properties of hydrocarbons and related compounds, Carnegie Press, Pittsburgh, 1953
Kuzman, R., - Tabele si diagrame termodinamice, Ed. Tehnica, Bucuresti 1978
Dobrinescu, D., - Procese de transfer termic si utilaje specifice, Ed, Didactica si Pedagogica, Bucuresti 1983
Zdonik, S.B., Green, E., Halle I., - Manufacturing ethylene, The petroleum Publ.Co.Tulsa Oklahoma, S.U.A. 1971
Anexa 1. Schema instalatiei de laborator de piroliza a hidrocarburilor lichide
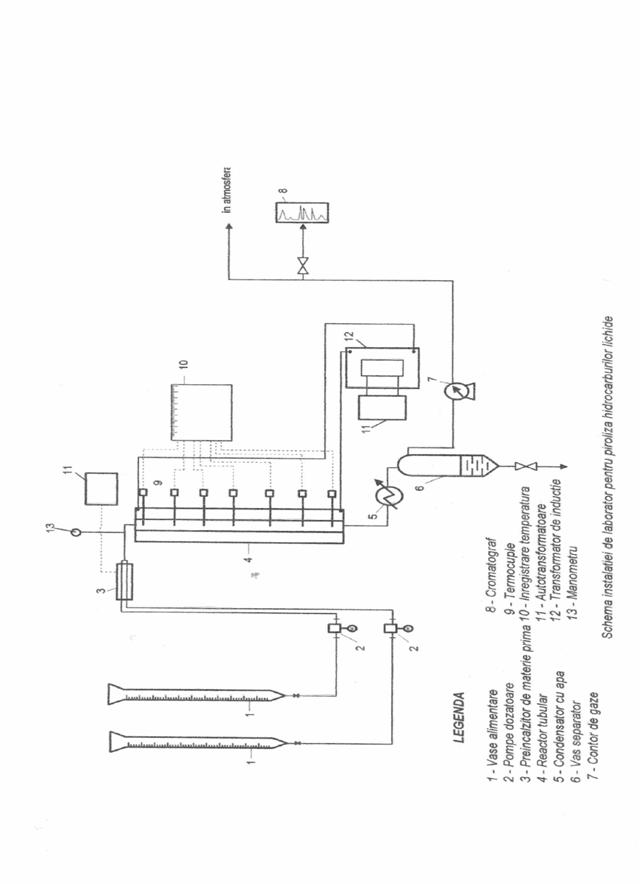
Anexa 2. Variatia constantei de viteza cu temperatura