a. Influenta carbonului
Proprietatile otelurilor carbon in starea de echilibru depind de natura si cantitatea fazelor si a constituentilor structurali de echilibru (diagramele de faze si structura din figura 9.13), care variaza cu continutul de carbon Din tabelul 9.4 s-a observat ca ferita imprima otelurilor plasticitate, tenacitate si feromagnetism; perlita - rezistenta, elasticitate si duritate; cementita - duritate si fragilitate.
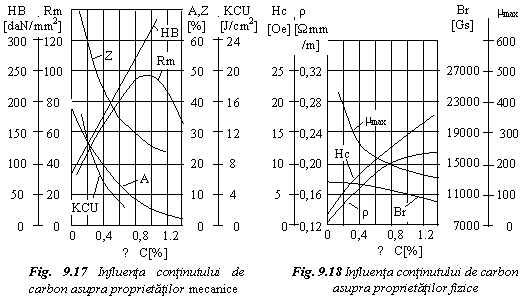 In figura 9.17 se
prezinta influenta carbonului asupra proprietatilor
mecanice.
In figura 9.17 se
prezinta influenta carbonului asupra proprietatilor
mecanice.
In domeniul hipoeutectoid, cresterea continutului de carbon produce marirea indicatorilor de rezistenta (rezistenta la tractiune Rm, duritatea Brinell HB), respectiv scaderea celor de plasticitate (alungirea specifica la rupere A, strictiunea Z) si de tenacitate (rezilienta KCU). Aceasta se coreleaza cu faptul ca, odata cu continutul in carbon, se mareste cantitatea de perlita si scade cea de ferita. In domeniul hipereutectoid apare cementita secundara, care determina marirea duritatii, dar reducerea plasiticitatii si tenacitatii. Rezistenta la tractiune prezinta un maxim la 0,9-1%C, pentru ca la continuturi mai mari de carbon cementita secundara se separa ca retea continua la limita grauntilor de perlita, cu efect fragilizant.
In figura 9.18 se prezinta influenta
carbonului asupra unor proprietati fizice. La cresterea
continutului de carbon scade cantitatea de ferita, se
mareste cantitatea de cementita si ca urmare se maresc
rezistivitatea electrica ρ, campul coercitiv Hc si se reduc
permeabilitatea magnetica μ si inductia magnetica
remanenta
Otelurile tehnice sunt aliaje polinare, care contin elemente insotitoare permanente in cantitati mici, care pot influenta sesizabil proprietatile otelurilor. Aceste elemente provin:
in urma reactiilor de dezoxidare (Si, Mn, Al);
din imposibilitatea eliminarii lor totale la elaborare (P, S);
din reactii cu faza gazoasa la elaborare sau turnare (O, N, H).
Siliciul se gaseste sub 0,5% in otelurile carbon. Siliciul provine din fonta bruta, captuseala cuptorului de elaborare, zgura si dezoxidarea otelului la elaborare.
Si + 2 FeO → SiO2 + 2 Fe
Siliciul se gaseste in otel dizolvat in ferita sau sub forma de incluziuni nemetalice (oxizi sau silicati). Prin dizolvare in ferita, siliciul o durifica, marind duritatea si rezistenta otelului.
Manganul este limitat la 0,8%. Se adauga la elaborare otelului in scopul dezoxidarii si desulfurarii acestuia.
Mn + FeO → MnO + Fe
Mn +
Prin substitutia fierului in sulfura de fier, Mn elimina fragilitatea la cald a otelului. De asemenea, Mn se gaseste in otel sub forma de incluziuni nemetalice ca: oxizi (MnO), sulfuri (MnS), silicati (MnO.SiO2, 2MnO.SiO2), contribuind la formarea fibrajului de deformare plastica si la anizotropia proprietatilor mecanice. In otelurile cu Mn spre limita superioara, deformate la cald, se ajunge la un raport 5/1 intre rezilienta longitudinala si transversala.
Manganul se dizolva in cementita, marind rezistenta si duritatea otelului. Cementita aliata cu Mn - (Fe,Mn)3C este usor solubila in austenita, favorizand cresterea grauntilor de austenita la supraincalzirea otelului.
Aluminiul este limitat la 0,03%. Se introduce la elaborare pentru dezoxidarea suplimentara a otelului.
2Al + 3 FeO → Al2O3 + 3Fe
Particulele submicroscopice de Al2O3, distribuite pelicular la limita grauntilor de austenita reprezinta o bariera mecanica, care impiedeca cresterea granulatiei austenitice la tratamentul termic sau la deformarea plastica la cald. Rezulta o granulatie secundara fina si marirea caracteristicilor de rezistenta, plasticitate si tenacitate a otelului. De asemenea aluminiul se introduce in otelurile de ambutisare pentru a elimina imbatranirea mecanica a otelului datorata azotului.
Fosforul este limitat in general la maxim 0,055%. Provine din minereuri si se indeparteaza la elaborare. Otelurile de convertizor sau de cuptor Martin bazic contin 0,02-0,04 %P. Otelurile de cuptor electric au cel mai redus continut de fosfor, sub 0,02%.
 Asa cum
reise din diagrama de echilibru Fe-P (fig. 9.19), fosforul se dizolva in
ferita pana la 1,2%. Raza atomica a fosforului este mult mai
mare decat a fierului, ceea ce produce o puternica deformare elastica
a retelei cristaline a fierului, cu efect de durificare si
scadere a tenacitatii otelului. La 0,3%P otelul este
foarte fragil, rezilienta fiind nula. Acest fenomen poarta
denumirea de fragilitate la rece.
Asa cum
reise din diagrama de echilibru Fe-P (fig. 9.19), fosforul se dizolva in
ferita pana la 1,2%. Raza atomica a fosforului este mult mai
mare decat a fierului, ceea ce produce o puternica deformare elastica
a retelei cristaline a fierului, cu efect de durificare si
scadere a tenacitatii otelului. La 0,3%P otelul este
foarte fragil, rezilienta fiind nula. Acest fenomen poarta
denumirea de fragilitate la rece.
Diagrama de echilibru releva un interval mare de solidificare, ceea ce determina la solidificare o tendinta marita de segregare a fosforului atat la nivelul lingoului (macrosegregatie pozitiva) cat si la nivelul dendritelor de austenita (microsegregatie dendritica). Zonele exterioare ale dendritelor de austenita vor rezulta mai bogate in P decat cele interioare.
Pe de o parte, segregarea P are drept consecinta formarea in zonele bogate in P (peste 0,25%P) a compusului Fe3P cu efect durificator si fragilizant. Zonele imbogatite in P sunt astfel zone cu duritate marita si tenacitate scazuta, provocand fragilitatea la rece a otelului. Cum segregatiile de P nu se pot elimina, se recurge la limitatea continutului de P. Astfel in otelurile carbon de calitate continutul de fosfor se limiteaza la 0,040%, iar la otelurile carbon de scule la 0,030%.
Pe de alta parte, segregarea P determina structura in siruri sau in benzi a otelului deformat plastic la cald. La deformarea plastica dendritele de austenita se alungesc si se orienteaza dupa directia efortului, contribuind la formarea fibrajului de deformare plasica. Cum fosforul micsoreaza solubilitatea carbonului in austenita, la racire zonele alungite, bogate in fosfor si sarace in carbon, vor fi sediul de germinare a feritei proeutectoide, iar zonele sarace in fosfor si mai bogate in carbon al perlitei. Apare dispunerea in benzi a feritei proeutectoide, respectiv a perlitei, care produce anizotropia caracteristicilor mecanice a otelului deformat la cald. Se poate preveni aparitia structurii in siruri prin deformarea plastica la temperaturi inalte, care faciliteaza omogenizarea chimica prin difuzie a carbonului.
Se utilizeaza continuturi mai mari in fosfor (0,10-0,15%P) la otelurile prelucrate prin aschiere pe masini unelte automate, deoarece prin efectul de fragmentare a aschiilor P imbunatateste prelucrabilitatea prin aschiere.
In otelul fosforos pentru piulite este un continut de 0,2-0,4%P in scopul cresterii duritatii si imbunatatirii rezistentei la uzare. Otelul are de asemenea o buna prelucrabilitate prin aschiere si o calitate deosebita a suprafetei prelucrate.
Se admite un continut mai mare de P in otelurile pentru poduri, pentru ca P impreuna cu Cu mareste rezistenta la coroziune atmosferica.
Sulful se limiteaza la maxim 0,045%. Sulful provine din minereu si din produsele de ardere ale combustibilului de la cuptoarele de elaborare. Cele mai reduse continuturi in S (<0,03%) se obtin la elaborarea in cuptoarele Martin bazic si electric.
 Conform diagramei
Fe-S (fig. 9.20) sulful nu se dizolva in fier. In absenta manganului,
sulful reactioneaza chimic cu fierul, formand sulfura de fier cu
temperatura de topire de 1190˚C.
Conform diagramei
Fe-S (fig. 9.20) sulful nu se dizolva in fier. In absenta manganului,
sulful reactioneaza chimic cu fierul, formand sulfura de fier cu
temperatura de topire de 1190˚C.
Fe + S →
Sulfura de fier
cristalizeaza ultima in procesul de solidificare al otelului, la
temperatura 985˚C, sub forma unui eutectic E (Feγ +
Otelul care contine
- fragilitate la rosu in intervalul 800-1000˚C, deoarece reteaua de eutectic intercristalin nu prezinta suficienta plasticitate;
- fragilitate la temperaturi ridicate, in intervalul 1000-1200˚C, deoarece eutecticul topit lasa fara coeziune grauntii de austenita.
Fragilitatea otelului la deformarea la cald se elimina prin desulfurare cu mangan. Sulful este legat chimic in sulfura de mangan, MnS, care este plastica si cu temperatura de topire ridicata (1610˚C). Continutul de Mn necesar desulfurarii este dat de relatia: [%Mn] = 1,72 [%S] +0,3. La <0,06%S este suficient 0,4%Mn.
Sulful este in cantitati mai mari (0,15-0,30%S) in otelurile prelucrate prin aschiere pe masini unelte automate, deoarece fragilizeaza aschiile si imbunatateste prelucrabilitatea prin aschiere.
Oxigenul este limitat la 0,05%. Provine la elaborare din contactul otelului topit sau la operatiile de incalzire din contactul otelului solid cu atmosfera oxidanta.
Oxigenul provenit de la elaborare se poate gasi in otel sub forma oxidului de fier FeO (wüstita), cat si sub forma oxizilor elementelor dezoxidante: MnO, CaO, Al2O3, SiO2. Acesti oxizi pot apare sub forma de incluziuni simple sau asociate, formand incluziuni de silicati (2FeO.SiO2; 3Al2O3.2SiO2) sau de spineli (FeO.Al2O3).
Oxigenul provenit din atmosfera de incalzire a pieselor si semifabricatelor din otel se gaseste sub forma de pelicule de FeO pe limita grauntilor de austenita. Stratul superficial oxidat intergranular (sau ars) este fragil si se rupe la deformare.
Incluziunile oxidice sau silicatii exogeni sunt incluziuni neplastice, in timp ce silicatii endogeni sunt incluziuni plastice. In otelul deformat plastic, incluziunile fragile se sfarama, cele plastice se alungesc si impreuna cu cele nedeformabile se distribuie in siruri discontinue in directia efortului. Incluziunile contribuie astfel la formarea fibrajului de deformare si la anizotropia caracteristicelor mecanice.
Proprietatile de utilizare sunt influentate defavorabil de prezenta incluziunilor nemetalice, care intrerup continuitatea masei metalice. Ele pot constitui amorse de fisura la oboseala si contribuie la ruperea fibruasa (la structura in siruri) sau la ruperea in terase (la distributia in placi a incluziunilor exogene masive).
Oxigenul se mai poate gasi in oteluri turnate si in stare gazoasa (O2, CO, CO2), determinand aparitia de sufluri. La deformarea plastica a otelului suflurile cu suprafata neoxidata se sudeaza prin presiune. In piesele turnate, prezenta suflurilor micsoreaza sectiunea utila, care preia efortul.
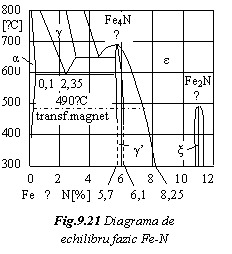 Azotul este limitat la
0,01% in otelul Martin si 0,03% la otelurile elaborate in cuptor
electric. Azotul difuzeaza in otel din atmosfera cuptorului. Asa
cum reiese din diagrama de echilibru fazic (fig. 9.21), solubilitatea azotului
in Feα este maxima de 0,1% la 590˚C si scade cu temperatura
la
Azotul este limitat la
0,01% in otelul Martin si 0,03% la otelurile elaborate in cuptor
electric. Azotul difuzeaza in otel din atmosfera cuptorului. Asa
cum reiese din diagrama de echilibru fazic (fig. 9.21), solubilitatea azotului
in Feα este maxima de 0,1% la 590˚C si scade cu temperatura
la
10-5 % la temperatura ambianta. De aceea, dizolvat in ferita la temperaturi ridicate, azotul se separa la racire sub forma de Fe4N (faza γ').
Prezenta azotului are o deosebita importanta mai ales la otelurile cu continut redus de carbon sub 0,15%C, deformabile la rece, deoarece provoaca imbatranirea mecanica a otelului. Daca dupa deformarea la rece si recristalizarea otelurilor, azotul se mentine dizolvat in ferita, in timp apare tendinta de separare spontana la temperatura ambianta din ferita suprasaturata in azot a azotului in exces. Procesul, numit imbatranire mecanica, se produce dupa cca 16 zile si este insotit de o puternica durificare si scadere a plasticitatii. Acest proces face ca otelurile susceptibile de imbatranire sa poata fi deformate plastic numai in primele 15-16 zile de la recristalizare. Imbatranirea produsa de azot se poate elimina prin dezoxidare cu aluminiu. La 0,03%Al intreaga cantitate de azot este legata chimic in nitrura de aluminiu, AlN. Nu mai exista astfel azot dizolvat in ferita, care sa participe la procesul de imbatranire.
Hidrogenul este prezent in otel in concetratii de ordinul procentelor per million (ppm). El poate proveni de la umiditatea unor materiale folosite la elaborare (ferosiliciu, var), din atmosfera cuptoarelor de incalzire sau de la decaparea cu acizi a suprafetei semifabricatelor.
Hidrogenul se gaseste in oteluri in stare atomica, dizolvat intersitial in ferita sau austenita. Solubilitatea hidrogenului in fier scade cu temperatura de la 0,003% in fierul lichid, la 0% la temperatura 200˚C. Datorita diametrului atomic mic, hidrogenul difuzeaza interstitial cu usurinta in fier, ceea ce permite la racire evacuarea in atmosfera. Daca timpul de evacuare este insuficient, hidrogenul ramas in otel, difuzeaza la defectele structurale (limite de graunte) sau la interfata cu incluziunile nemetalice, unde isi reface starea moleculara, cu o puternica crestere de volum si aparitia de tensiuni interne. Aceste tensiuni pot depasi local limita de rupere a otelului provocand aparitia de microfisuri, numite fulgi, datorita aspectului stralucitor, luminos, pe suprafata de rupere a otelului. Fulgii se formeaza la temperatura de 200˚C in piesele sau semifabricatele de dimensiuni mari, racite rapid, dupa deformarea plastica la cald. Formarea lor se elimina prin: evitarea umiditatii materialelor folosite la elaborare, prin racirea lenta pana la temperatura ambianta sau prin mentinerea izoterma la temperaturi peste 200˚C pana la evacuarea completa a hidrogenului in stare atomica.
In cazul curatirii suprafetei de oxizi prin decapare cu acizi, hidrogenul dizolvat in exces formeaza sufluri de decapare, care contin hidrogen molecular. Sub ambele forme, fulgi sau sufluri, hidrogenul micsoreaza tenacitatea otelului.